1. インピーダンスと電池の基礎
2025年8月13日の CO2 濃度は、 推定450ppm。 この100年間で、地球大気中の二酸化炭素の 濃度は1.4倍になった。 前史時代の二酸化炭素濃度は、280ppmでほぼ一定だった。 石炭 を使い始めた産業革命から指数的に増加を始めた。 石油を使い始めてからは指数項が加わった。
日本の 炭素強度は、580gCO2eq/kWh
今、地球がヤバい。 脱炭素社会 には 再生可能エネルギー の活用が必須。そのためには、 電気エネルギーを 備蓄 する電池が必須なのだ。
- 国土交通省、気象庁 二酸化炭素濃度の経年変化 https://ds.data.jma.go.jp/ghg/kanshi/ghgp/co2_trend.html
- 東北大学大学院理学研究科 大気海洋変動観測研究センター 過去250年間の大気中二酸化炭素濃度の変動 http://caos.sakura.ne.jp/tgr/observation/co2
電池の電圧は電流に比例せず、線形システムではありません。 一方、インピーダンスはシステムの線形性を仮定します。 まずは、電池の起電力や内部抵抗など基本的なところをおさらいして、 インピーダンス測定とどう折り合いをつけるかみてみましょう。
1.1 電池の起電力と内部抵抗
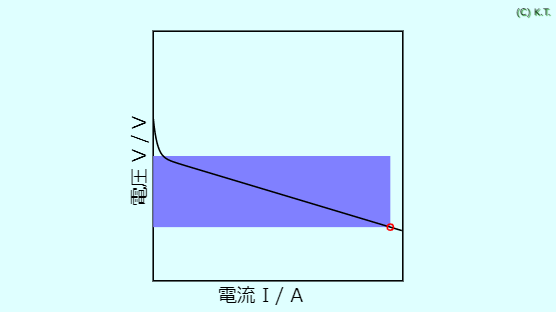
◇電池は電気を流さなくても電圧があります。これを電池の起電力といいます。このときの内部抵抗は無限大とみなせます。電池から電流を取り出すと電圧が下がります。この見かけの抵抗を内部抵抗と呼びます。
コイン電池(人間電池)の起電力

てのひらに、10円と1円をのせれば、 電気化学の三要素 がそろって、電池になります。 デジタル式回路計で、 電圧を測定すると、0ではありません。 これが 電池の起電力です。 電流が流れていないにもかかわらず電圧があるのです。 電池では、電流と電圧が、そのまま比例しません。 電池は単なる電気抵抗ではないのです。 化学反応が電気を起こしているのです。 11円電池は、 ガルバニ電池と言っていいでしょう。
ネルンストの式
酸化体が多いほど、酸化力(電位)が上がります。 電位は、ネルンストの式で説明されます。
ネルンストの式
電池の起電力と内部抵抗
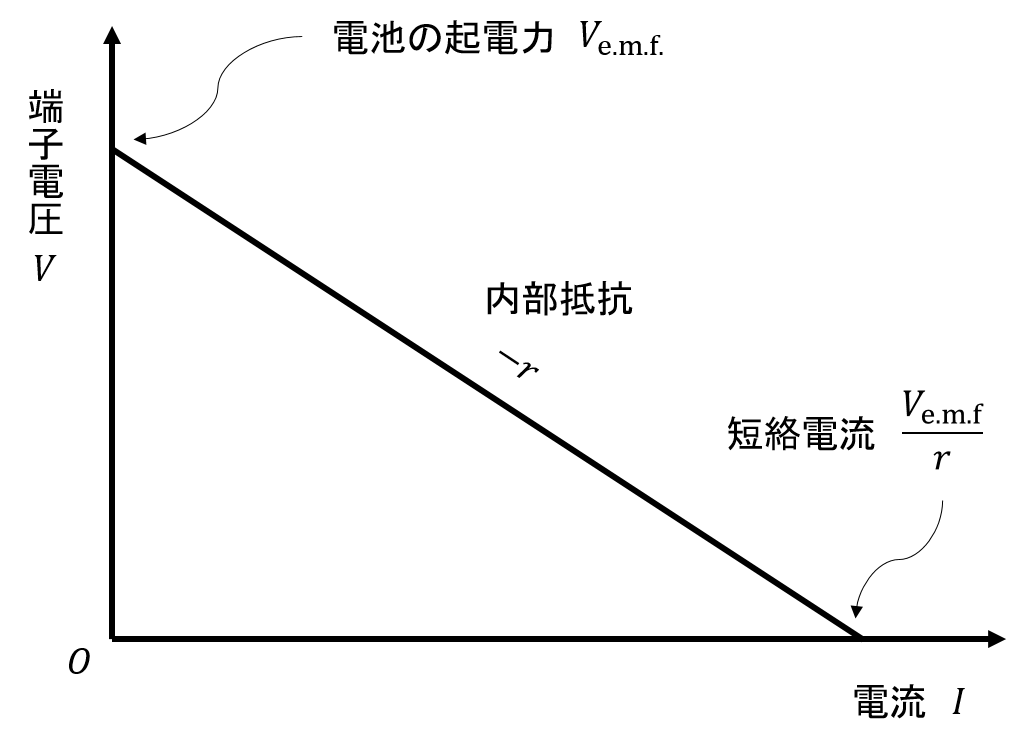
電池の起電力は、正極と負極の単極電位の差です。 単極電位は、おおむね ネルンストの式に従います。 ネルンストの式によれば、電位は、活量に依存します。 このことは電池反応の進行とともに、電位が変化することを意味します。 逆に言えば、端子電圧から、電池の起電力を推定し、 電池の残量(SOC)を推定することができます。 2 )
電池の端子電圧は、流れる電流が増えると小さくなります。この電流増加に対する電圧降下の割合を電池の内部抵抗と言います。
電池と内部抵抗と等価回路
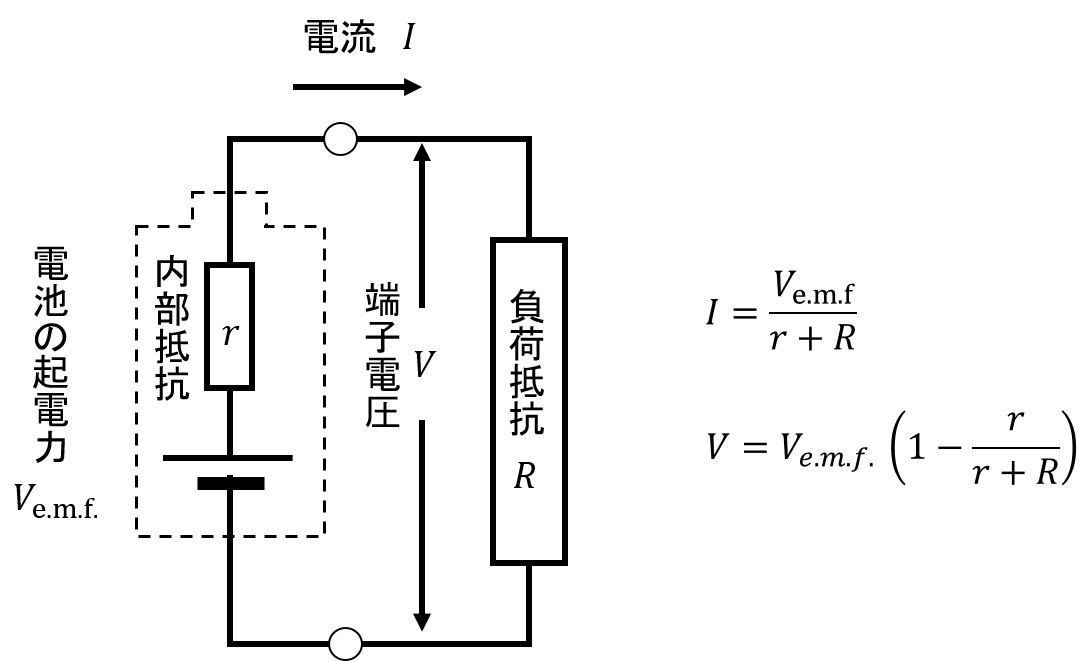
電池は、化学エネルギーを電気エネルギーに変換するデバイスです。 その変換効率は高いほど良いです。 変換損失は熱エネルギーとなって放出されます。 この発熱は変換効率を悪化させるだけでなく、電池の温度を上昇させ、電池の安全な動作を妨げます。 電池の発熱は、内部抵抗rという 等価回路で表現されます。 電池の端子間電圧Vは、電池の起電力Ve.m.f.より電圧降下Irを差し引いた電圧です。
電流と電圧と電気抵抗の関係
電池の発熱は、電流の二乗×内部抵抗。 発熱は、無駄な発電負荷であり、無駄な二酸化炭素の排出。 大型電池ほど、放熱が不利になり、熱暴走のリスクが高まります 電池の内部抵抗を下げることが、脱炭素社会への道。
過電圧(電圧降下)=活性化過電圧+濃度過電圧+抵抗過電圧(溶液抵抗+接触抵抗)
電気量と電圧と静電容量の関係
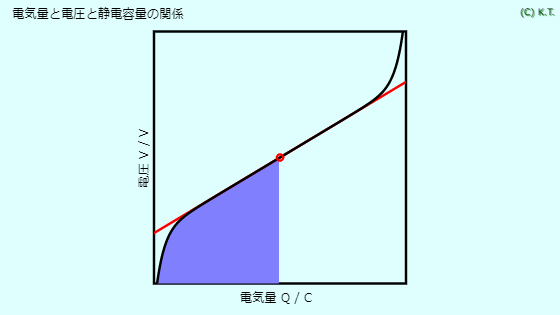
理想的なコンデンサ(キャパシタ)では、電圧は電気量に比例します。
その比例計数が静電容量です。
理想的な電池では、電圧は一定です。なので静電容量は∞です。
実際の電池では、
回路計で測れる物理量
| 物理量 | 単位 | 備考 |
|---|---|---|
| 電圧 V | V | 乾電池の 開回路電圧は1.65V。 乾電池 の公称電圧は1.5V。 ダニエル電池の 起電力は、1.1V 水の理論分解電圧は1.23V。 |
| 電流 I | A |
豆電球の電流は
0.5A。
ぽちっと光ったLEDの電流は1mA。
電流密度=電流÷電極面積
|
| 時間 t | s | |
| 電気量 Q | C |
🖱 電気エネルギー は 電気量×電圧 |
| 電気抵抗 R | Ω |
,
|
| 静電容量 C |
|
,
|
| インダクタンス L |
|
,
|
回路計は、電圧、電流、電気抵抗などを測定できます 3 ) 。
電気抵抗、静電容量、インダクタンスを実現する電子部品( 回路素子)として 抵抗器、コンデンサ(キャパシタ)、コイルがあります 4 ) 。
⚖️ 電圧 V〔V〕 ⚖️ 電流 I〔A〕 ⚖️ 電気抵抗 R〔Ω〕電位プロファイル―正極と負極-
均一固相反応(S字)と二相(L字)反応
正極活物質の反応は、 大きく均一固相反応と二相反応に分類されます。 MnO2やLCOは、均一固相反応と言えます。NiOOHやLFOは二相反応と言えます。 均一固相反応の放電曲線はS字型を描き、二相反応の放電曲線はL字型を描きます。 放電深さにおける起電力はネルンストの式で議論でいます。 バッテリーマネジメント の立場から言うと、S字型の放電曲線は、電圧だけで 残量管理ができるメリットがあります。 しかし負荷からすれば電池の電圧が変動してしまうデメリットもあります。
1.2 電池の構造とインピーダンス
◇ ◇EVのバッテリーシステム

バッテリー、セル、電極
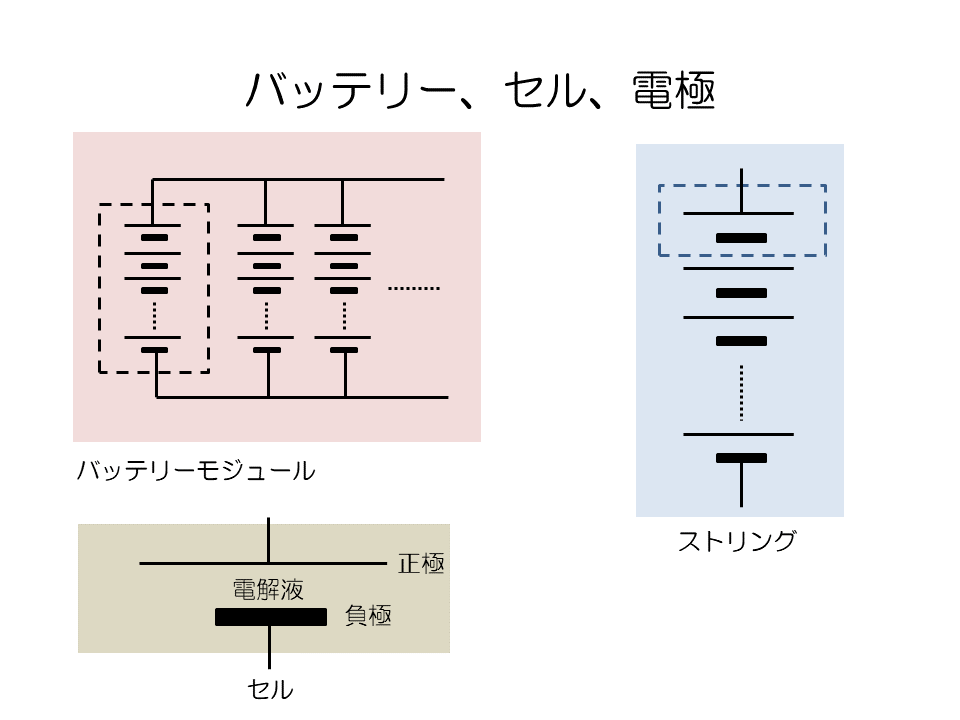
セルの種類
| 分類 | 種類 | 備考 | |
|---|---|---|---|
| セル(単電池) | 二極式 フルセル | 実用電池(コインセル、円筒型電池)、メッキ試験(ハルセル)、電解槽など。 アノード、 カソードのみ | |
| 三極式 ハーフセル | 作用極 、対極、 参照極 | ||
|
バッテリー(組電池) 電解槽 |
単極式(モノポーラ) | ||
| 複極式(バイポーラ) | 液を通しての短絡電流を防ぐなどの工夫が必要となる。 トヨタ 古河電池 |
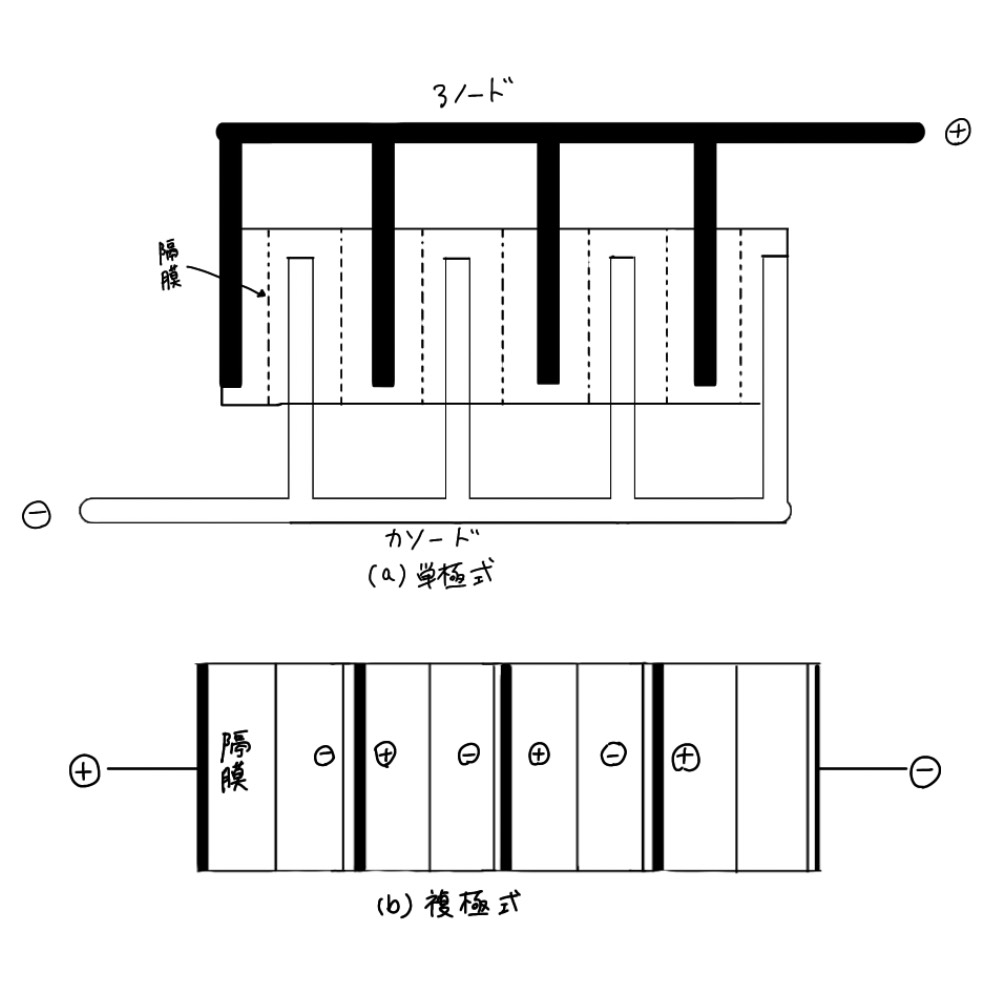 図
10
.
電極の接続様式
図
10
.
電極の接続様式
バイポーラ接続では、ブスバーなどの重量を低減できるため、 バッテリーだけでなく、 水電解の電解槽などでも、応用が考えられるが 液絡のリスクを減らすのが課題です。 5 )
セルとセル定数

物質に電気を流すには、 電極を少なくともふたつ取り付けなくてはいけません。 電極ふたつがついた一組を、セルと呼びます。 電解槽、電気化学セル、電池などセルと言います。 セルは電気エネルギーを使った反応器です。
セルには細胞という意味もあります。
ひとつあるいは複数のセルを直列につないで電気と取り出すひとかたまりとした場合の電池は、バッテリーと呼びます。
セルには寸法があります。 セルの寸法でうち大切なふたつは、電極面積と電極間距離です。 電極面積と電極間距離の比をセル定数と言いますが、実際のセルでは複雑なカタチをしているので、セル定数を実験的に定めることが多いです。 また電極面積も、電極表面に微細な凹凸があったりすると、真の電極面積とみかけの電極面積が異なります。 真の電極面積とみかけの電極面積の比を、拡面倍率と呼んだりします。
導電率 などを測定するセルでは、白金黒(こく)などで電極表面で加工して、拡面倍率を大きくして、電極表面インピーダンスを小さくして、導電率測定の精度を向上させます。
平行平板電極であれば、
セル定数a=電極間距離d÷セル断面積S
です。
一般的には、導電率既知のKCl溶液などを使って、セル定数を較正します。
コンダクタンス=導電率
電気抵抗=抵抗率×長さ÷電極面積
セル定数と物性
| 物理量 | 単位 | 凡例 |
|---|---|---|
| 電極間距離 d | m | 電界の強さ=電圧÷電極間距離 |
| セル断面積 S | m² | 拡面倍率1で、平板モデルのとき電極面積≒セル断面積 |
| 電極面積 A | m² | 実験室でよく使う旗型電極の電極面積は 1cm²。 |
| セル定数 a | 1/m |
セル定数a=電極間距離d÷セル断面積S コンダクタンス G = 導電率 σ ÷セル定数 電気抵抗=抵抗率ρ×セル定数a |
| バルク電流密度j | A/m2 | バルク 電流密度 j = 電流I÷セル断面積 |
| 界面電流密度j | A/m2 | 界面 電流密度 j = 電流I÷電極面積 |
| 電界の強さe | V/m | 電界の強さe = 電圧V÷電極間距離 |
電池の表記と特性(電池式)

-
立花和宏、仁科辰夫.
電池式の書き方と電極の呼び方
. 山形大学, エネルギー化学 講義ノート, 2015. https://edu.yz.yamagata-u.ac.jp/developer/Asp/Youzan/@Lecture.asp?nLectureID=4304 , (参照 ).
電池と電池式
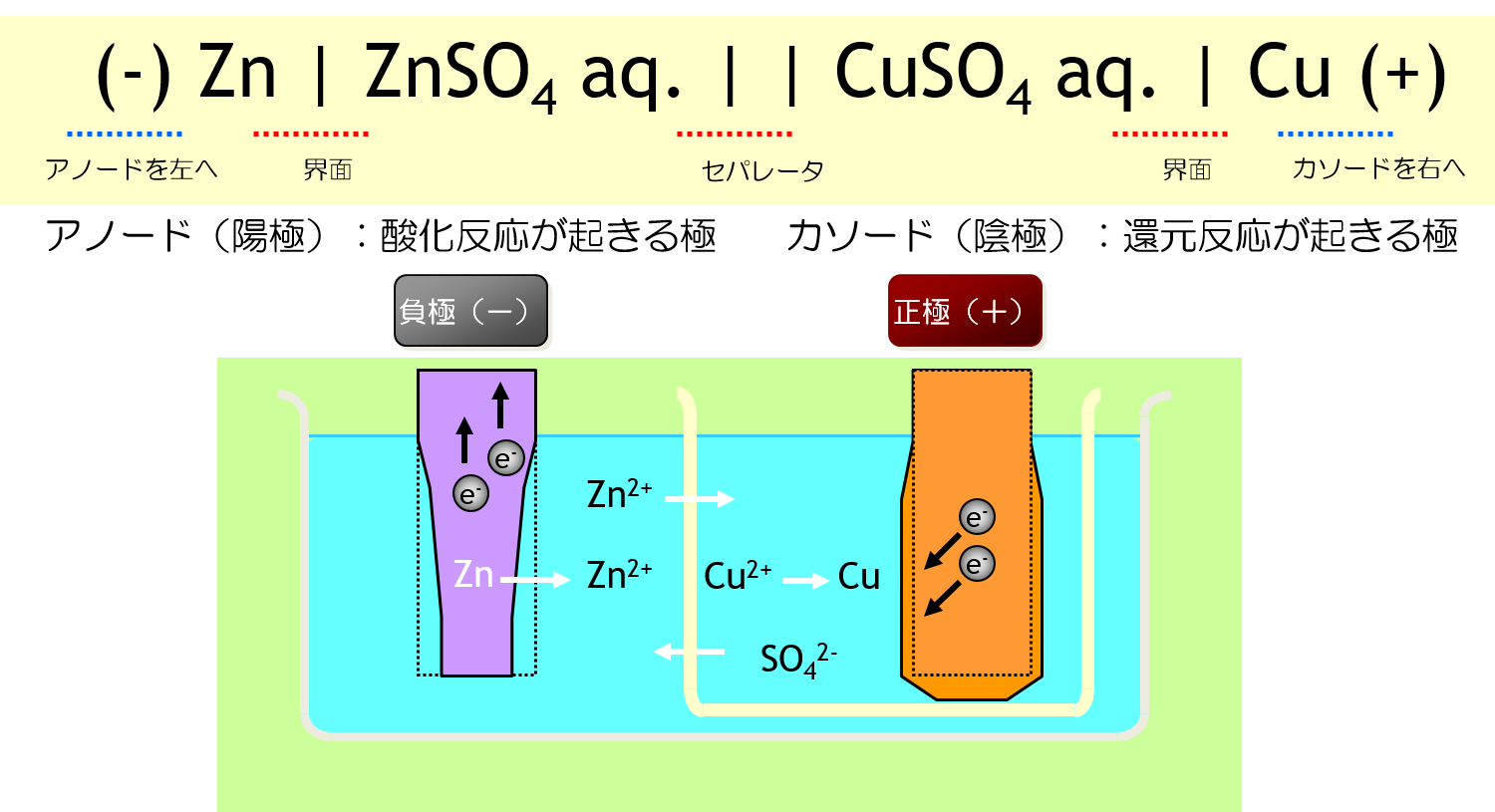
ダニエル電池の模式図
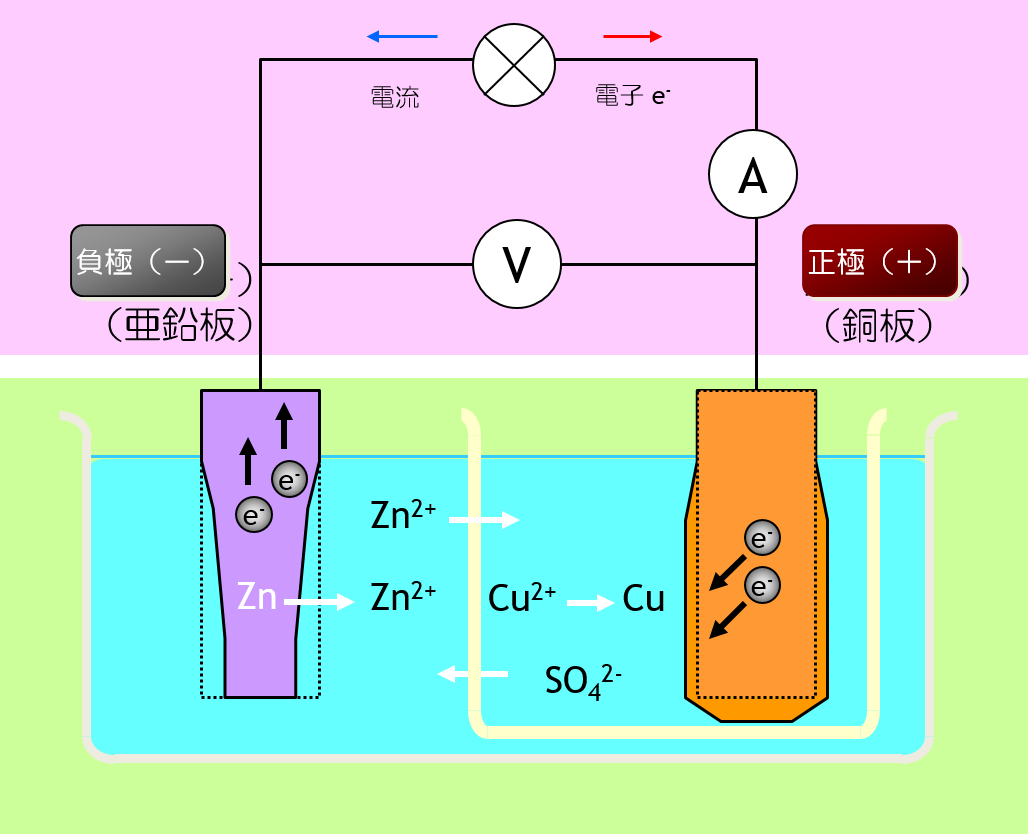
ダニエル電池の動作
ガルバーニ電池、 ボルタ電堆、 ダニエル電池と発展します。
ダニエル電池では、正極も負極もカタチが変形するのです。 しかも、カタチの変形が可逆でないのです。 可逆でないカタチの変形は、充電式電池(二次電池)にとって、致命的です。
乾電池の模式図
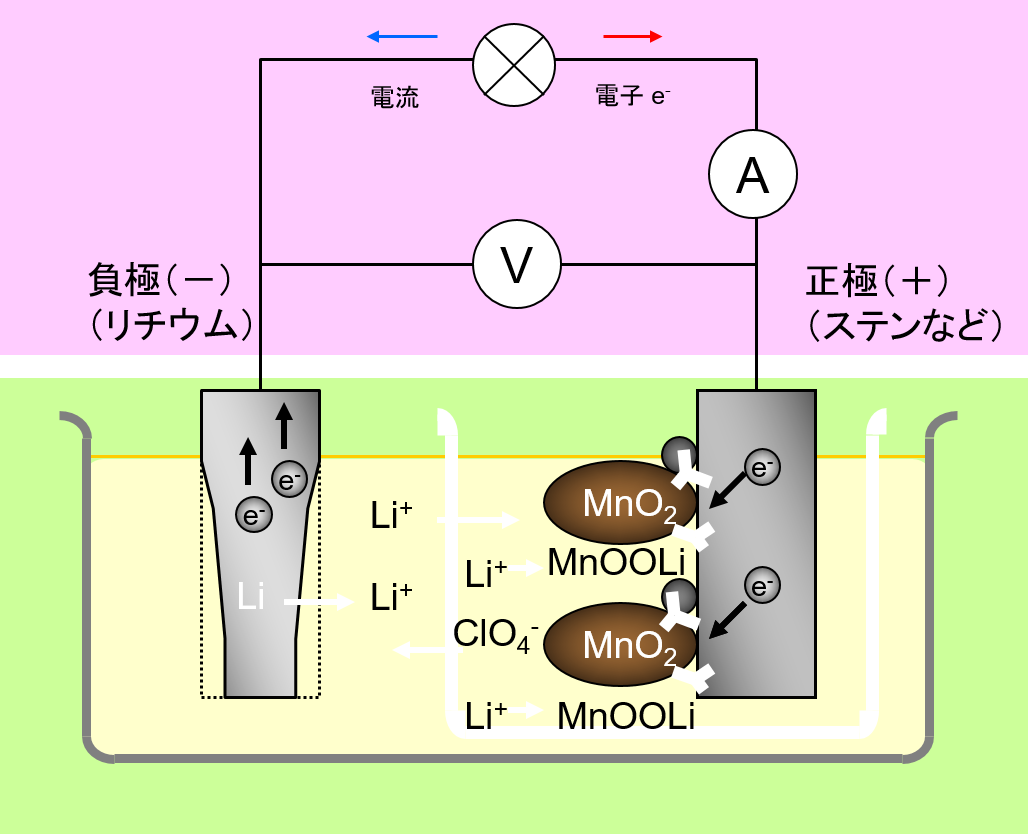
リチウム電池の模式図
リチウムイオン二次電池
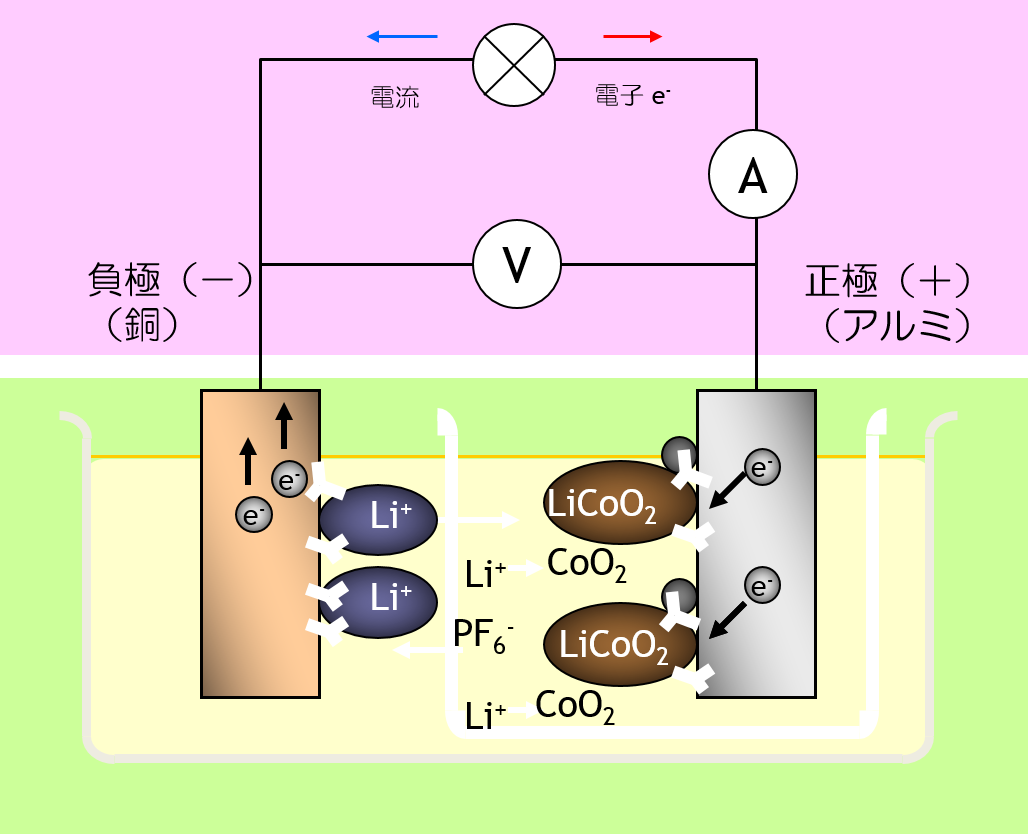
リチウムイオン二次電池 では、 正極活物質も 負極活物質も、 固相反応にすることでカタチが変形を最小限にしています。 しかし、反応生成物の化学組成が違う以上、密度が変化するので、カタチの変形から逃れることはできません。 カタチの変形によって、固体と固体の 接触状態が変わるため、 電池の内部抵抗の増大の原因になります。
リチウムイオン二次電池
リチウムイオン電池の正極と負極
リチウムイオン電池は、 正極集電体に正極合材、負極集電体に負極合材があって、それぞれ、 正極と 負極となります。 セパレータを介して電解液を挟みます。 活物質、導電助剤、バインダーなどを合材スラリーとして集電体上に、塗布し、乾燥して、電極とします。
電池を動物に例えるなら
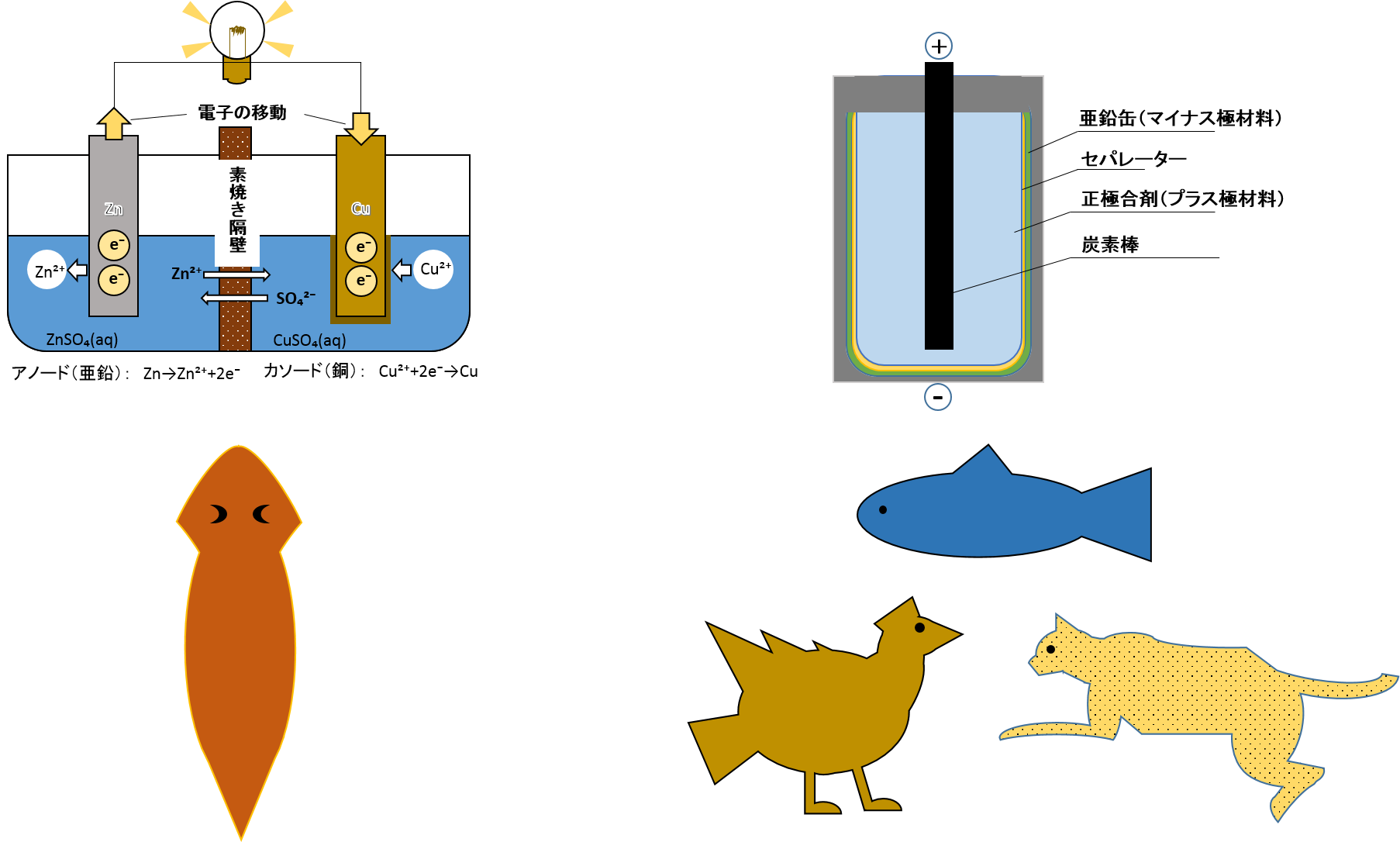
電池を動物に例えるなら
| ダニエル電池 | 乾電池 | |
|---|---|---|
| 動物 | ブラナリア | 脊椎動物 |
| 呼吸 | 体表呼吸 | 肺呼吸 |
| 集電体 | なし | 分離 |
| 循環系 | なし | 閉鎖血管系 |
| 電極 | 電極表面 | 複合電極 |
| 排出器 | 体表 | 腎臓 |
| 等価回路 | 単純 | 分布定数回路 |
リチウムイオン二次電池の正極(放電時カソード)の構造
正極では、 正極合剤は、 正極活物質、 導電助剤、 バインダー( PVdF、NMP)を混錬したスラリーからなり、 正極集電体に塗布・ 乾燥されている。 電池 の放電時は、 正極活物質にチウムイオンと電子が吸収され(電荷移動過程)、それぞれ導電助剤と電解液を通る。
電池材料リチウムイオン二次電池の負極(放電時アノード)の構造
負極では、 負極合剤は、 負極活物質、 導電助剤、バインダー(SBR、CMC、水)を混錬したスラリーからなり、 負極集電体 に塗布・乾燥されている。 電池 の放電時は、負極活物質からリチウムイオンと電子が放出され、それぞれ導電助剤と電解液を通る。
1.3 材料物性値とインピーダンス
◇インピーダンスから物性値へ(バッテリー、セル、界面とバルク)
電池、界面特性、物性値
|
計測可能
な
物理量
(セル) |
界面
の特性値 (面積) |
バルクの
物性値
(セル定数) |
|---|---|---|
|
電気抵抗
R[Ω]
=電圧÷電流
,
|
反応抵抗(面積抵抗率)
Rct〔Ωm-2〕
=電圧÷ 表面 電流密度 接触抵抗 (界面抵抗) * =電圧÷表面電流密度 |
抵抗率(体積抵抗率)ρ
=電場強度e÷ 断面 電流密度 抵抗率ρ〔Ωm〕=電気抵抗R〔Ω〕÷ セル定数 a〔1/m〕 電気抵抗R=抵抗率ρ×長さl/面積S 7 ) 抵抗率ρ=1÷導電率 |
|
コンダクタンスG[S]
=1÷電気抵抗R |
導電率
σ(
|
|
|
静電容量
(キャパシタンス)C
,
|
電気二重層容量Cd〔Fm-2〕 |
誘電率
=電荷密度÷ 電場強度e |
|
インダクタンスL
,
|
透磁率 μ |
電池の内部抵抗は、 バルク抵抗だけでなく、界面抵抗に左右されます。 溶液に金属を浸しただけの ダニエル電池 のような単純な電池では、バルク抵抗が支配的ですが、 合材電極や固体電解質を使う リチウムイオン電池 のような複雑な電池では、界面抵抗が支配的です。 電池の内部抵抗の評価には、 交流評価と直流評価を組み合わせが必要です。
界面とバルク―等価回路―
電池 は、 アノード、 カソード、電解質の 三要素 からなります。 電池で起きる現象は、 電解質などの バルクの現象、 アノードやカソードといった電極と電解質の 界面の現象に、分けられます。
界面を表す 特性とバルクを表す 物性があります。等価回路ではときどき不明瞭なものがありますので、単位で確認しましょう。
たとえばバルクの測定をメインにする導電率測定の導電率計では、 界面インピーダンスを下げるため、電極に300倍もの拡面倍率を持つ白金黒電極を使います。
界面を表す特性とバルクを表す物性があります。等価回路ではときどき不明瞭なものがありますので、単位で確認しましょう。
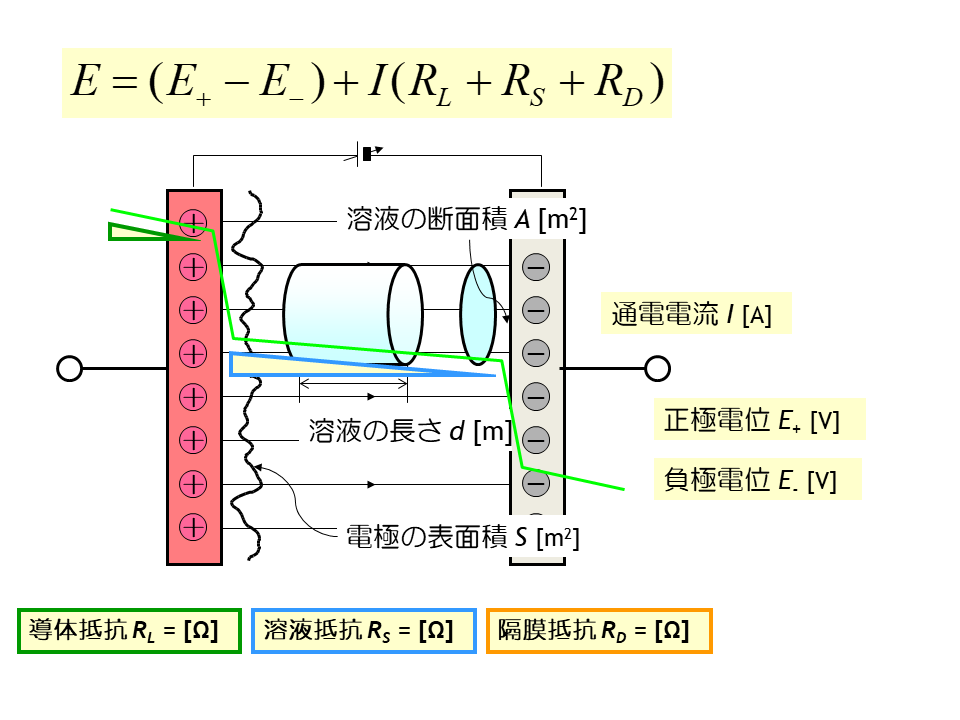
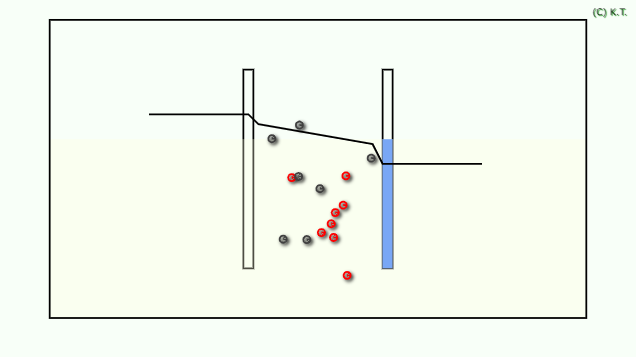
電池のモデル溶液抵抗と電位プロファイル
電解液の溶液抵抗
種々の界面
| 固体 | 液体 | 気体(真空) | |
|---|---|---|---|
| 固体 |
面接触(例:
pn接合) 線接触(三相界面)(例:正極合材、 局部電池) 点接触(三相界面 ショットキー接触 )(例:固体電解質、 炭素導電助剤粒子 ) |
固液界面 (例:サスペンジョン) | 表面 |
| 液体 | 固液界面 (例:電極と電解液) | 液液界面 (例:エマルション) | 気液界面 ( 表面 ) |
| 気体(真空) | 表面 | 気液界面 ( 表面 ) | (混合) |
物質は、 様々な状態をとります。 界面や表面 は、ある材料の相と異なる材料の相が接するところです。
電池の内部抵抗は、バルクと界面との両方から生じます。
固体は、形状が決まっているので、接触界面に多様性がある。
接触抵抗 内部抵抗粒界界面の存在

粒子界面(点接触)の存在
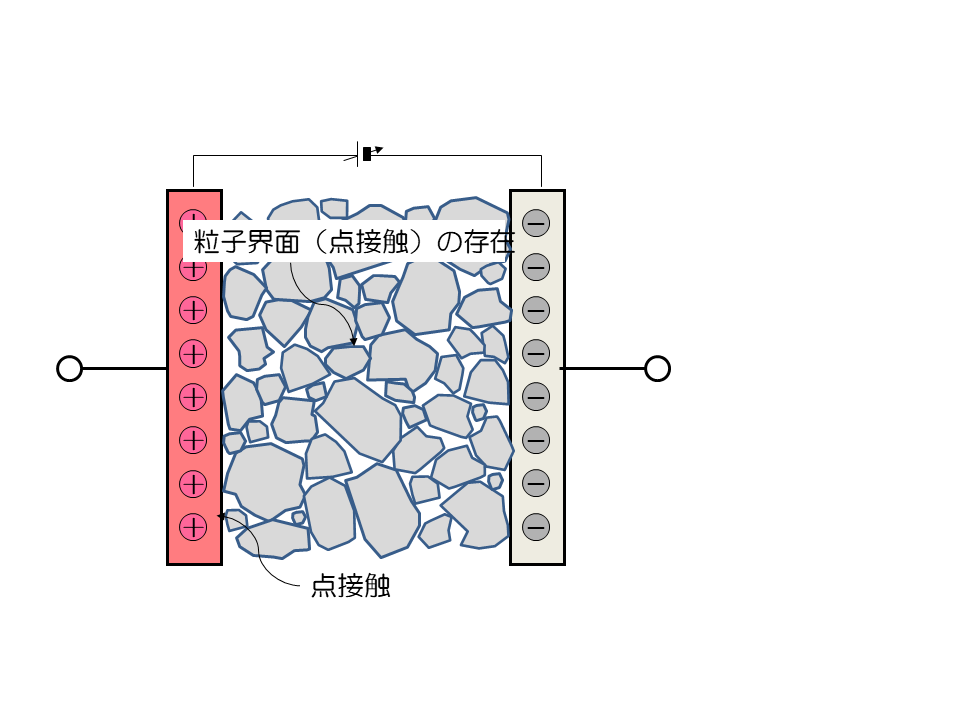
固体粒子の接触は、点接触です。面積を見積もるのがとても大変です。界面の電流密度がわかりません。 接触抵抗は電流集中を伴うので、圧縮などの影響を受けやすいのです。活物質や炭素材料、固体電解質などの取り扱いが難しいのはそのためです。
電極内部の界面の数
実用電池のほとんどは電極内部に複雑な構造を持ち、多種の材料からなる。 たとえば活物質、導電助剤、バインダー、電解液、集電体としただけで その界面の組み合わせは5C2=20通りに達するのである。 このような電極に単純な等価回路を当てはめて議論するのは無理があり、 かといって等価回路を複雑にしたところで意味がない。
回路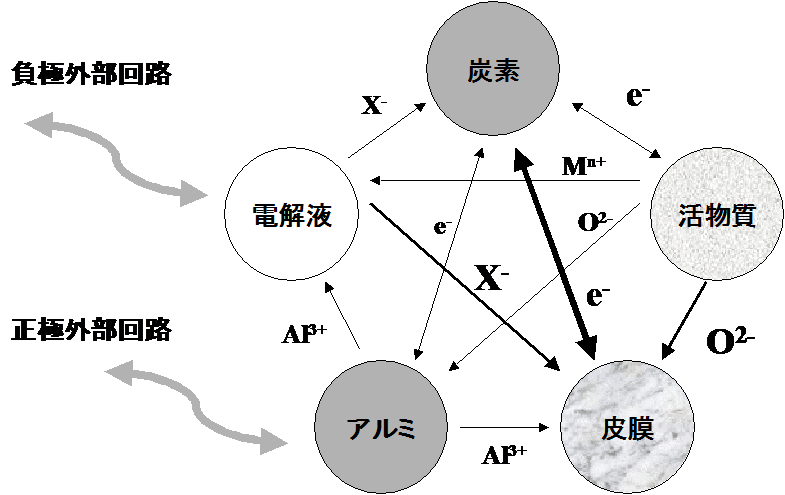
バルクの物性値-導電率、誘電率-
1.4 ボーデプロットとコールコールプロット
◇コールコールプロット(ナイキストプロット)とボードプロットはインピーダンス測定結果の主要な表現です。とボードプロットにはしばしば両対数プロットが使われます。
コールコールプロットとナイキストプロット交流の電流と電圧の比を インピーダンスと言います。
インピーダンス は複素数なので、実部と虚部があります。 実部をリアクタンスと言い、虚部をレジスタンスと言います 8 ) 。 各周波数での インピーダンスの軌跡を複素平面上にプロットしたものを コールコールプロットあるいはナイキストプロットと言います。
*パイソンで描いたコールコールプロット
インピーダンスに出てくる諸元
インピーダンスは数式1で示されます。
| 物理量 | 数式 | 備考 | |
|---|---|---|---|
| 周期 T〔s〕 | 🖱山のてっぺんからてっぺんまでの時間です。 | ||
| 周波数 f〔Hz〕 | f = 1/T | 周波数と振幅で交流を表現します。 | |
|
角周波数
|
ω=2πf | ||
| 電圧 振幅Ep0 | 交流の大きさの表現には、振幅のほかにピークトゥピークや実効値があります (※)。 | ||
| 電流 振幅Ip0 | |||
| インピーダンス Z〔Ω〕 | * | ||
| 絶対値 |Z| | |||
|
位相角
|
|||
| アドミタンス Y〔S〕 | * | ||
| インダクタンス L | |||
| 静電容量C | |||
| 電気抵抗 R | インピーダンス Z の実部 | ||
| リアクタンス X | インピーダンス Z の虚部、 X=ωL-1/ωC | ||
| コンダクタンスG | アドミタンス Y の実部 | ||
| サセプタンス B | アドミタンス Y の虚部 |
インピーダンスブリッジや インピーダンスブリッジメーターで 測定します。
⚖️ 周波数 ⚖️ 電圧 ⚖️ 電流複素平面にプロットしたインピーダンスの周波数による軌跡を コールコールプロットまたは ナイキストプロットと呼びます。
-
1.
インピーダンスと電池の基礎
- 1.1 電池の起電力と内部抵抗
- 1.2 電池の構造とインピーダンス
- 1.3 材料物性値とインピーダンス
- 1.4 ボーデプロットとコールコールプロット
-
3.
インピーダンスと数学
- 3.1 フーリエ変換とそのファミリー
- 3.2 離散変換とサンプリング
- 3.3 数式処理ソフトの活用
- 4. 電池のモデル作成