 🏠
🏠
 🏠
🏠

てのひらに、10円と1円をのせれば、 電気化学の三要素 がそろって、電池になります。 デジタル式回路計で、 電圧を測定すると、0ではありません。 これが 電池の起電力です。 電流が流れていないにもかかわらず電圧があるのです。 電池では、電流と電圧が、そのまま比例しません。 電池は単なる電気抵抗ではないのです。 化学反応が電気を起こしているのです。 11円電池は、 ガルバニ電池と言っていいでしょう。
| 物理量 | 単位 | 備考 |
|---|---|---|
| 電圧 V | V | 乾電池の 開回路電圧は1.65V。 乾電池 の公称電圧は1.5V。 ダニエル電池の 起電力は、1.1V 水の理論分解電圧は1.23V。 |
| 電流 I | A |
豆電球の電流は
0.5A。
ぽちっと光ったLEDの電流は1mA。
電流密度=電流÷電極面積
|
| 時間 t | s | |
| 電気量 Q | C |
🖱 電気エネルギー は 電気量×電圧 |
| 電気抵抗 R | Ω |
,
|
| 静電容量 C |
|
,
|
| インダクタンス L |
|
,
|
回路計は、電圧、電流、電気抵抗などを測定できます 1 ) 。
電気抵抗、静電容量、インダクタンスを実現する電子部品( 回路素子)として 抵抗器、コンデンサ(キャパシタ)、コイルがあります 2 ) 。
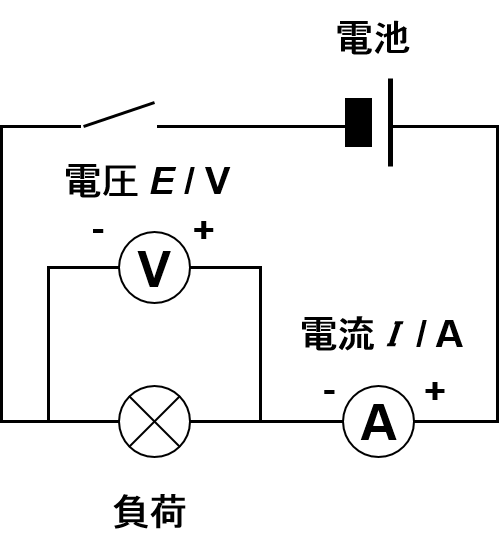
電気回路図の記号は電気用図記号は JISで定められており、考えたところでもムダなので、読み書きを練習して慣れるしかありません。
電気化学系の最小単位は、一つの電子伝導体Mと一つのイオン伝導体Sの接触によって構成されます 3 ) 。
電解質は、電子絶縁体です。 電池で、電子絶縁破壊が起きると、電気分解です。 コンデンサでは、電子絶縁体は、誘電体です。
電気を流すには最低2つの電極が必要です。電池でもキャパシタでも2つの電極の電圧を測定することから始まります。
| 注目する量 | 電極の名称 | 説明 |
|---|---|---|
| 電位 に注目 | 正極 | 電位の高い電極、(+)プラス。 正極活物質 は、電池放電時に、酸化剤。 |
| 負極 | 電位の低い電極、(-)マイナス。 負極活物質 は、電池放電時に、還元剤。 | |
| 電流に注目 | アノード | 電流が流れ込む電極。酸化反応が起きる電極。 放電するときは負極。 充電式電池では、充電のときは正極。 |
| カソード | 電流が流れ出る電極。還元反応が起きる電極。 放電するときは正極。 充電式電池では、充電のときは負極。 |
電池には電極があります。酸化が起きる極をアノード、還元が起きる極をカソードと呼びます。 以前はアノードを陽極、カソードを陰極と呼びましたが、正極と陽極がまぎらわしいのでアノードと呼びます。 アノードは電流が外部回路から流れ込む極です。カソードは電流が外部回路へ流れ出す極です。 アノード、カソードは電流の向きに注目した呼び方です。 それとは別に正極と負極という呼び方があります。 電位の高い極を正極、電位の低い方を負極と呼びます。 正極、負極は電位の高低に注目した呼び方です。
| 電池 | 電池式 | 性質や特色 | |
|---|---|---|---|
| 歴史的電池 |
1800
ガルバノ電池 (ボルタ電堆) |
Zn|H2SO4aq|Cu | 銅は単なる集電体。正極活物質は酸素。 |
| ダニエル電池 | Zn|Zn2+aq||Cu2+aq|Cu | 正極活物質と負極活物質が分離。集電体は反応系を兼用 | |
| 一次電池 | 1888 乾電池 6 ) | Zn|NH4Claq|MnO2, C|C | 正極活物質に酸化物(固体)とバインダーを採用。正極合材。 負極活物質の 亜鉛は両性金属なので、アルカリに溶けてしまう。 |
| 1950 アルカリ乾電池 | Zn | KOHaq | MnO2 ,C | Ni | ||
| 1970 リチウム電池 | Li | LiClO4,PC | MnO2,C | SUS304 | 有機電解液 採用。 | |
| 二次電池 | 1991 リチウムイオン電池 7 ) | (-) Cu | C | LiPF6,EC+DEC | LiCoO2, C | Al (+) | |
| 鉛電池 | 鉛は両性金属だが、硫酸には溶けない。 | ||
| ニカド電池 * | Cd|Cd(OH)2|KOH aq|NiOOH | 亜鉛と違って カドミウムは両性金属でないのでアルカリに溶けない。 | |
| ニッケル水素電池 | MH|KOH aq|NiOOH | 水素吸蔵合金はアルカリに溶けない。 | |
イタリアの解剖学者Lugi Galvani(1737-1798)は、蛙の解剖に端を発した二つの異種金属を接触させたときに流れる電流を動物電気と称した(1979)。 この現象は直ちに同国のAlessandoro Count Volta(1745-1827)により追試され、ボルタの電堆として実証された(1800年3月)。 Galvaniの業績をたたえてこの種の電池を ガルバニ電池と呼んでいる。
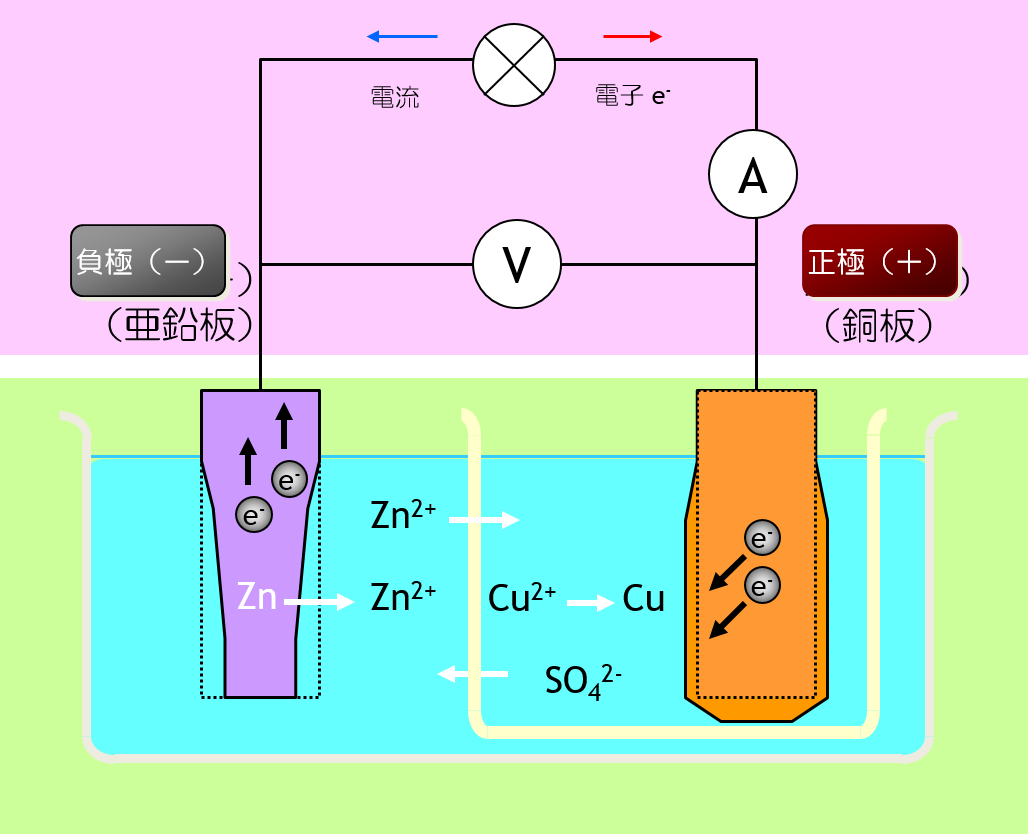
| 電池式 | Zn | ZnSO4aq || CuSO4aq | Cu |
| 負極 反応 | Zn2+ + 2e- ← Zn Eº = -0.7626V |
| 正極 反応 | Cu2+ + 2e- → Cu Eº = 0.34V |
| 全反応 | Zn +Cu2+ → Zn2+ + Cu |
| 起電力 | e.m.f. = 1.1026V |
| 理論容量 ( 電力原単位 ) | 415.7mAh/g |
| 理論重量エネルギー密度 13 ) | 458.4mWh/g |
起電力は、電解液中の亜鉛イオンと銅イオンの活量が1であるとしたときの起電力です。 関与する化学種の活量を全て1としたとき、起電力は、酸化還元電位の差になります。
*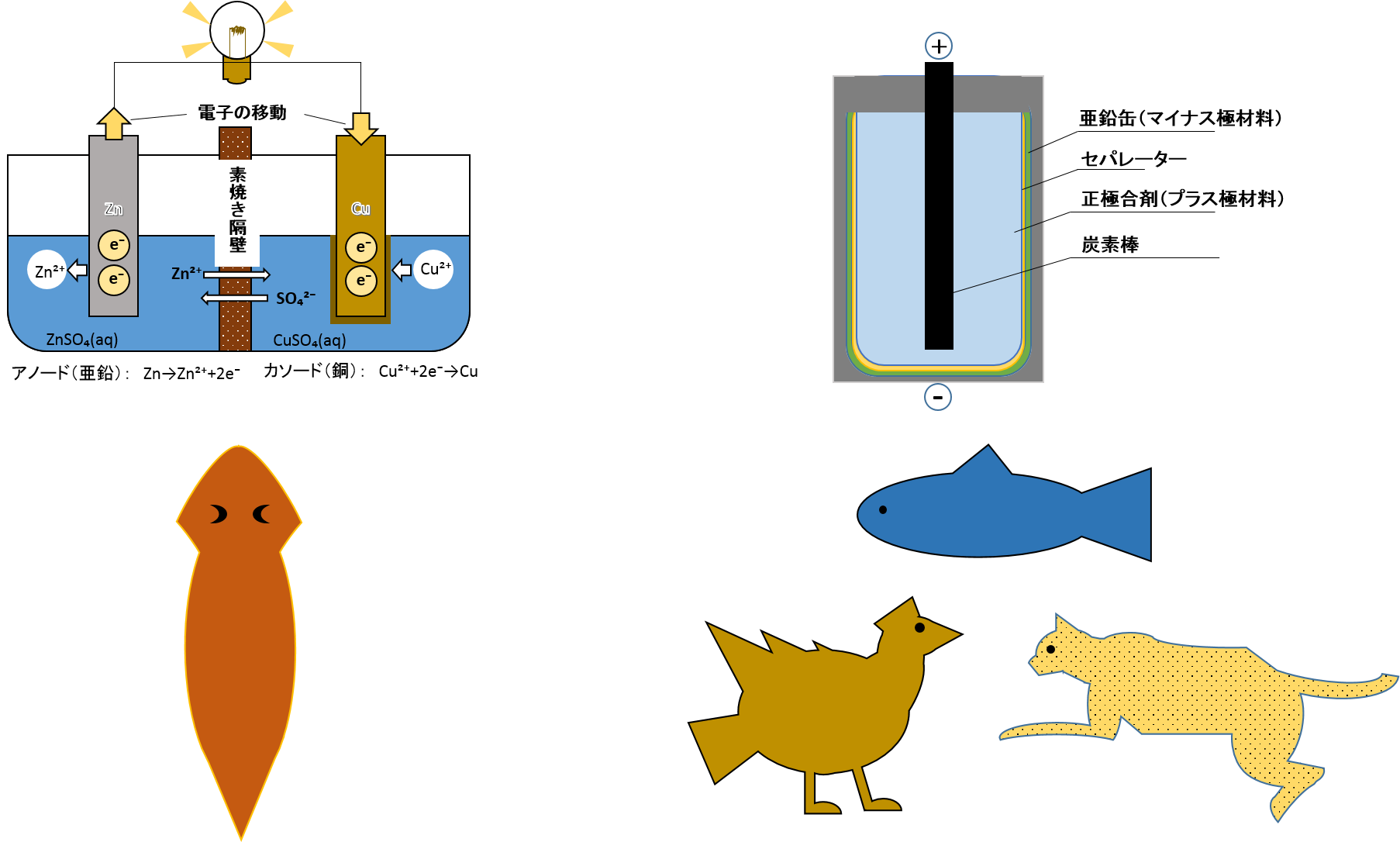
| ダニエル電池 | 乾電池 | |
|---|---|---|
| 動物 | ブラナリア | 脊椎動物 |
| 呼吸 | 体表呼吸 | 肺呼吸 |
| 集電体 | なし | 分離 |
| 循環系 | なし | 閉鎖血管系 |
| 電極 | 電極表面 | 複合電極 |
| 排出器 | 体表 | 腎臓 |
| 等価回路 | 単純 | 分布定数回路 |
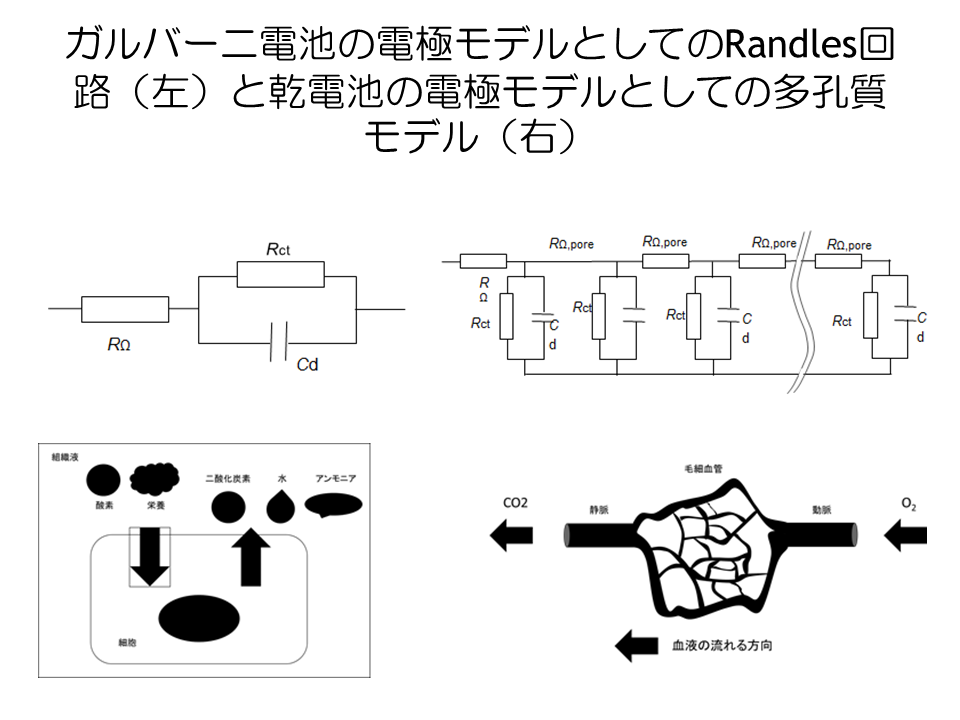
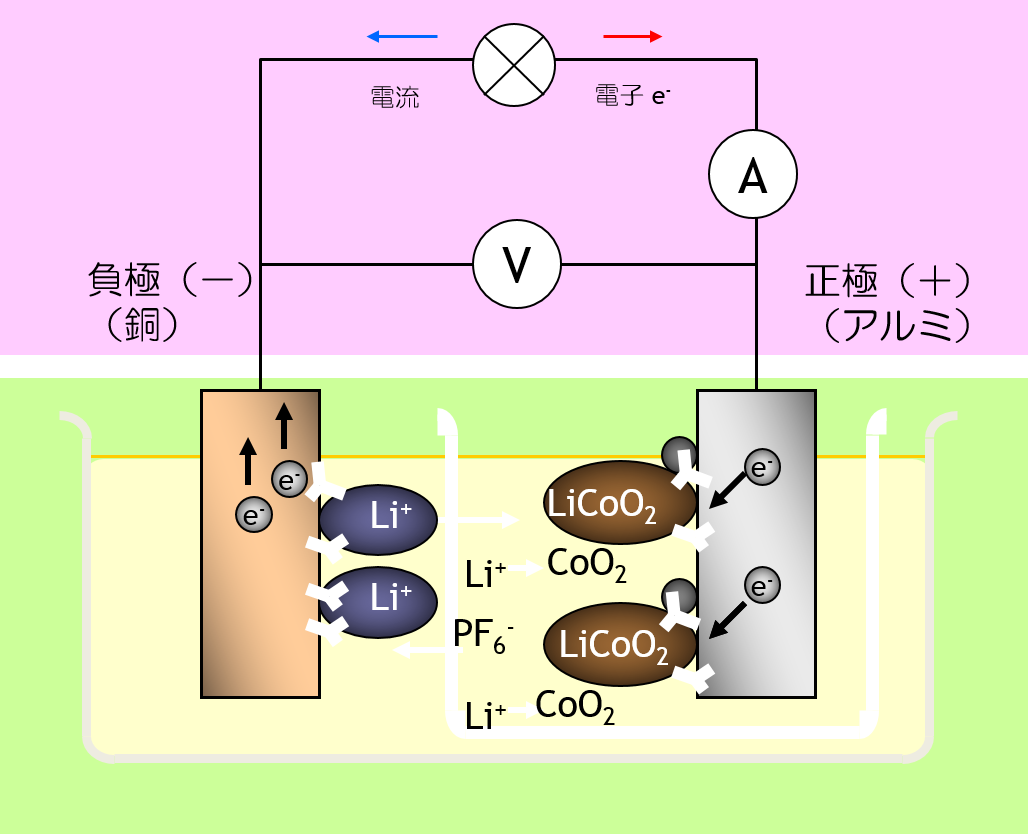
リチウムイオン二次電池 では、 正極活物質も 負極活物質も、 固相反応にすることでカタチが変形を最小限にしています。 しかし、反応生成物の化学組成が違う以上、密度が変化するので、カタチの変形から逃れることはできません。 カタチの変形によって、固体と固体の 接触状態が変わるため、 電池の内部抵抗の増大の原因になります。
| 電池式 |
組み立て後:Cu|C|LiPF6 EC+DEC|LiCoO2
,C|Al 充電後:Cu|C6Lix|LiPF6 EC+DEC|Li1-xCoO2 ,C|Al |
| 負極 反応 | 6C+xLi++xe-=C6Lix Eº = -3V |
| 正極 反応 | LiCoO2=xLi++xe-+Li1-xCoO2 Eº = 0.7V |
| 全反応 | |
| 起電力/V | 3.7 (公称電圧) 18650リチウムイオン電池は1セルの公称電圧が3.6Vまたは3.7V |
| 最低放電終了電圧/V | 2.5~2.75V |
| 実用電池容量/mAh | 1200~3300mAh |
| 理論電池容量/mAh | |
| サイクル寿命/回 | |
|
理論重量容量密度
( 理論容量 ・ 電力原単位 ) /mAh/g |
157.7mAh/g |
|
理論重量エネルギー密度
/mWh/g |
583.5 |
| 実用 重量エネルギー密度 | 200~250Wh/kg 程度 * |
| 形状・寸法 | 円筒型 (18650の例 18は直径18mm、65は長さ65mm、0は円筒形) 2170や4680も * * 、 ラミネート型 |
| 重量 | |
| 用途 | 住宅、 自動車、 スマホ |
14 ) https://led-outdoorgear.biz/wp/18650-pse/ F=96485.33212331
ジェリーロール構造は、スパイラル電極構造とか捲回型とも言われます。 円筒型電池には、出力重視のスパイラル電極構造のほかに容量重視のボビン電極構造もあります。 * さらに出力重視では、ラミネート型電池に使われる枚葉積層型があります。 * * 電極面積を大きくし、電極間距離を小さくして、電解液による溶液抵抗を減らし、 内部抵抗を小さくします。
リチウムイオン電池は、 正極集電体に正極合材、負極集電体に負極合材があって、それぞれ、 正極と 負極となります。 セパレータを介して電解液を挟みます。 活物質、導電助剤、バインダーなどを合材スラリーとして集電体上に、塗布し、乾燥して、電極とします。
正極では、 正極合剤は、 正極活物質、 導電助剤、 バインダー( PVdF、NMP)を混錬したスラリーからなり、 正極集電体に塗布・ 乾燥されている。 電池 の放電時は、 正極活物質にチウムイオンと電子が吸収され(電荷移動過程)、それぞれ導電助剤と電解液を通る。
電池材料負極では、 負極合剤は、 負極活物質、 導電助剤、バインダー(SBR、CMC、水)を混錬したスラリーからなり、 負極集電体 に塗布・乾燥されている。 電池 の放電時は、負極活物質からリチウムイオンと電子が放出され、それぞれ導電助剤と電解液を通る。
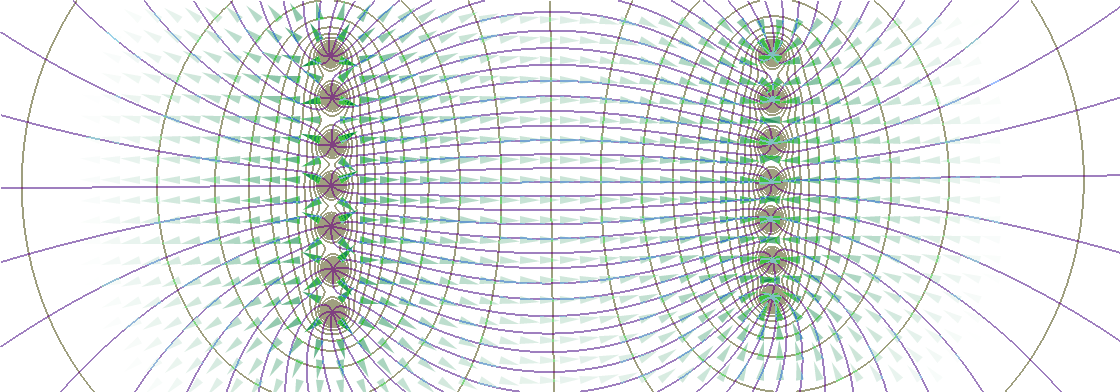
等電位線(等電位面)は、平面上(空間中)の電位の等しい点をつないだ線(面)です。 等電位線は、気象の天気図の等圧線、地図の等高線と同じ概念と思ってさしつかえありません。
大きな平行板電極を小間隔で向かい合わせると、電界の強さおよびその方向が、均一になります。 これを平等電界と言います。 でも、板の端の部分では電界が両電極板の外側に出る形になり平等電界ではなくなります。 この現象を端効果たんこうか(縁効果えんこうか)と言います。 https://em.ten-navi.com/dictionary/1763/
電池には電極があります。
酸化が起きる極をアノード、還元が起きる極をカソードと呼びます。 以前はアノードを陽極、カソードを陰極と呼びましたが、正極と陽極がまぎらわしいのでアノードと呼びます。 アノードは電流が外部回路から流れ込む極です。カソードは電流が外部回路へ流れ出す極です。 アノード、カソードは電流の向きに注目した呼び方です。 それとは別に正極と負極という呼び方があります。 電位の高い極を正極、電位の低い方を負極と呼びます。 正極、負極は電位の高低に注目した呼び方です。
ダニエル電池を放電するときは、負極の亜鉛が酸化して亜鉛イオンになります。 つまり負極がアノードです。 乾電池の負極も亜鉛です。 乾電池に豆電球をつないで点灯させているときも亜鉛が亜鉛イオンとなって溶け出していることになります。
| 分類 | 材料 | 特徴 |
|---|---|---|
| 電極材料 | 正極材料 (活物質) | 極性固体、 酸化物、 イオン結合、 絶縁体 |
| 負極材料 (活物質) | 極性固体(金属やグラファイト)/非極性固体(酸化物) | |
| 導電材 | 非極性固体 炭素材料 | |
| 分散剤 | 界面活性剤 | |
| ◇ バインダー | 界面活性剤 | |
| CMC・増粘剤 | 極性材料 | |
| 集電体 (金属) | 非極性固体 | |
| 電解質 | 電解液、添加剤* | |
| セパレータ | ||
| その他 | 外包材・リードタブ |
界面は、 極性どうし、あるいは非極性どうし、だとなじみがいい。 異なる界面では、なじみが悪いので、界面活性剤などを検討する。
2024年1月21日 松木健三名誉教授がご逝去されました。