 🏠
🏠
 🏠
🏠
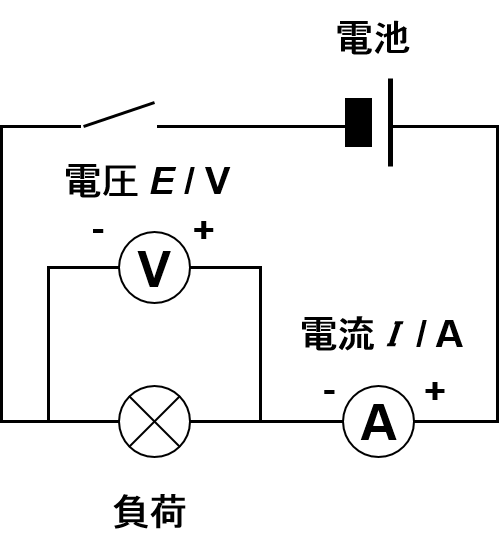
電気回路図の記号は電気用図記号は JISで定められており、考えたところでもムダなので、読み書きを練習して慣れるしかありません。
電池、結線、スイッチ、電球、 電気抵抗、 コンデンサ、 コイル、電圧計、電流計、検流計などは最低限覚えましょう。
| 物理量 | 単位 | 備考 |
|---|---|---|
| 電圧 V | V | 乾電池の 開回路電圧は1.65V。 乾電池 の公称電圧は1.5V。 ダニエル電池の 起電力は、1.1V 水の理論分解電圧は1.23V。 |
| 電流 I | A |
豆電球の電流は
0.5A。
ぽちっと光ったLEDの電流は1mA。
電流密度=電流÷電極面積
|
| 時間 t | s | |
| 電気量 Q | C |
🖱 電気エネルギー は 電気量×電圧 |
| 電気抵抗 R | Ω |
,
|
| 静電容量 C |
|
,
|
| インダクタンス L |
|
,
|
回路計は、電圧、電流、電気抵抗などを測定できます 1 ) 。
電気抵抗、静電容量、インダクタンスを実現する電子部品( 回路素子)として 抵抗器、コンデンサ(キャパシタ)、コイルがあります 2 ) 。
たとえば、 電気抵抗は、物体やデバイスの 特性値ですが、 抵抗率は、 物質の量によらない物質固有の 物性値 です。
⚖️ 電圧 V〔V〕 ⚖️ 電流 I〔A〕 ⚖️ 電気抵抗 R〔Ω〕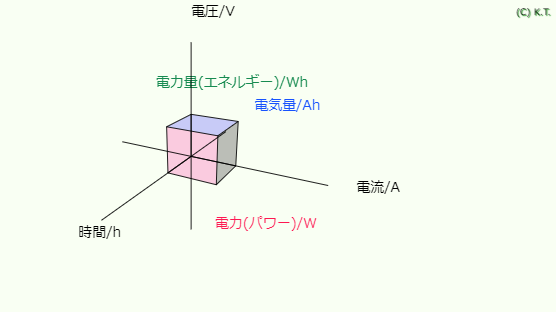
電気エネルギー(電力量)〔Wh〕=電圧〔V〕×
◇電気量〔
電気エネルギー〔Wh〕=電圧〔V〕×
◇電流〔
動力・電力・パワー〔W〕とエネルギー・電力量〔Wh〕は、絶対に間違わないようにしましょう。
⚡ 電気( n F E , e Φ) ⚡ 電気エネルギー E センサー 機器分析 物性電気量を測るには、電析した物質量を測ればいいのです。
「どんだけ強力な還元剤を使ったとしてもカリウムを単離することは不可能だろうね」
「ならどうやって単離したんですか?」
「電気分解さ。ボルタの電堆を使ってデービーはカリウムを単離することに成功したんだ」
「なるほど」
「単離できたとなれば、次やりたいのは量産だよね」
「うんうん」
「ファラデーっておっさんが、地道な実験を積み重ね、1832年に
電気分解によって析出する
物質量n
が通電した
電気量
Q
と
に比例することを見出した」
式で書くとこうなる。
96485.332 〔 C/mol 〕 は、アボガドロ数×電気素量で、それらはSIで定められた 定義定数 です。
工業的には、 26.801 〔 Ah/mol 〕をよく使います。
ファラデー定数は、 エネルギー密度や理論容量の計算にも使います。
このファラデー定数F=96485こそ、物質量と電気量を橋渡しするマジックナンバー、ファラデー定数です。 目にも見えず、触れてもわからない電気の量を、物質の目方を測ることで定量したのです。
| 表現 | |
|---|---|
| ネルンストの式 |
|
| ファラデー電気分解の法則 |
|
ファラデー定数F は物質量あたりの、電気素量eは粒子あたりの、電気量Qを表現します。
96485 C/mol より 27 Ah/molが便利です。
⚡ 電気( n F E , e Φ)| 項目 | 平衡論 | 速度論 | |
|---|---|---|---|
| 🧪 化学 ( G ) | 平衡定数 | 反応速度 | |
| ⚡ 電気( n F E , e Φ) | 起電力 | 分解電圧 | |
| 🔥 熱( R T, kB T, ) | 熱力学 |

物質量n〔mol〕と 電気量n〔C〕 は比例します。これを ファラデーの電気分解の法則と言います。 比例定数はファラデー定数F=96485.3415〔C/mol〕です。 定義定数です。 工業的には、ファラデー定数F=26.801〔Ah/mol〕 をよく使います。
ファラデーの法則を使って電気量を測る装置を クーロメーターと言います 5 ) 。 銀クーロメーター 6 ) 、 1936年の レイリー型電流天秤 7 ) を経て、現在の電気基準になりました。 産業界では、実用上、ツェナダイオード電圧標準器と標準抵抗器を 標準 としています。
| 電池系/電解系 | 電池式 | 備考 | |
|---|---|---|---|
| 亜鉛の単極電位 | R.E. (+) Ag| AgCl | Cl- | sat. KCl aq || Zn2+ | Zn (-) W.E. | ||
| ダニエル電池 | Zn | Zn2+ || Cu2+ | Cu | ||
| リチウムイオン二次電池 | Cu|C6Li|LiPF6 EC+DEC|□CoO2,C|Al | ||
|
銅の電解精錬 /銅めっき / 銅クーロメーター |
アノード ( + ) Cu | Cu2+ | Cu ( - ) カソード Cu|CuSO4aq|Cu | ||
| 希硫酸の電気分解 ( 水電解) | アノード ( + ) Pt | H2SO4 | Pt ( - ) カソード | ||
|
アルミニウムの アノード酸化 |
Al| Al2O3 | NH4OOC(CH2)4COONH4 aq | ||
| 銀のアノード酸化 | Anode(+) Ag|AgCl|HCl aq | Pt (-)Cathode |
電池式では、 界面を縦棒(|)で表します。


電気量を測る装置は電量計またはクーロメーターと呼びます。 ボルタメーターと呼ぶこともありますが、ボルトメーターと紛らわしいので使わない方がいいでしょう。 クーロメーターは測ろうとする電流を電解液に通じて、電気分解をして、析出した金属または気体の量を測り、 ファラデーの電気分解の法則を使って、通じた電気の量を知る装置です。つまり、電流計を較正する装置です。 主なクーロメーターとしては銀クーロメーター、銅クーロメーター、爆鳴気クーロメーターがあります。
電気量を測る装置を電量計またはクーロメーター(coulometer)とよぶ。またこれをボルタメーター(voltameter)とよぶことがあるが、この名はボルトメーター(voltmeter)と紛らわしくてよくない。何クーロンの電気が流れたかを測る器であるから、クーロメーターとよぶ方が適当である。
クーロメーターは、測ろうと思う電流を電解質水溶液に通じて電気分解を行わせ、析出した 金属または 気体の 量を測り、 ファラデーの法則を用いて、そのとき通じた電気の量を知る装置である。
鮫島実三郎. 物理化学実験法 より 8 )
電流が流れると近くにある方位磁針が振れます。 電流に測る方法があるのか?それは流れた電気量と流した時間から決めることができます。

米沢高等工業学校本館から 銀電量計を探してみよう。
米沢高等工業学校本館 応用化学科展示室(会計室) に展示してあります。
🏛️ 👨🏫 🗿銅クーロメーターは銀クーロメーターほど正確でないけれど、材料が安く便利なため広く使われます。 ビーカーに銅板を浸し、一方をアノード、もう一方をカソードとします。 欲組成の例としては150グラムの硫酸銅、50グラムに硫酸および50グラムのアルコールを水1000グラムと混ぜたもの。 空気があると銅が酸化する恐れがあるので、空気が液中に溶けるのを追い出すために、二酸化炭素または水素を細いガラス管で送ります。 電流密度はカソード1平方センチにつき2~20ミリアンペア程度。カソードは使用の前に一度電流を通じて、表面に新たに銅を付着させ、 それを水洗い、アルコールで洗い乾かし、秤量し、測るべき電流を通じます。
1クーロンの電気で遊離される銀の質量はいくらか?また銅の質量はいくらか?また0度1気圧での爆鳴気の体積はいくらか?


電気分解を使って物質を作ったり、純度を高めたりすることができます。 物質を作る電解製造としては、食塩を作るときの電気透析、食塩電解の塩素、アルミニウム精錬のアルミニムなどがあります。 また純度を高めることでは銅の電解精製がよく知られています。
ただ実際には通電した電気量がすべて目的の物質量とはなりません。目的の物質が析出した割合を電流効率といいます。また平衡電位から求めた目的の物質の理論分解電圧よりよけいにかけた電圧を過電圧と言い、槽電圧のうち理論分解電圧の割合を電圧効率といいます。
電解精練(粗銅を陽極、純銅を陰極として電気分解を行う)の工程を施すことで、電気銅と呼ばれる純度99.99%の銅が得られる。
野村正勝・鈴鹿輝男. 最新工業化学より
アノードもカソードも銅だったら、理論分解電圧は何Vになるか?
| プロセス |
アルミ ニウム 溶融塩電解 |
食塩電解
( ソーダ工業 ) |
銅 電解精錬 |
亜鉛 電解採取 |
|---|---|---|---|---|
| 🏞 原料 | 食塩(岩塩) | |||
| 製品 | 亜鉛 | |||
| 理論電気量 /kAh/t | 2980 | 670 | 844 | 820 |
| 理論分解電圧 /V | 4.17 | 2.2 | 0.1×10-3 | 2.0 |
| アノード 電流密度/A/m2 | ||||
| 単槽 電圧/V | ||||
| 電気量原単位 /kAh/t | 3350 | 910 | ||
| 電解電力 ( 電力原単位 ) /kWh/t | 13400 | 2200 | 284 | 3000 |
| 電流効率 | ||||
| 電圧効率 | ||||
| エネルギー効率 10 ) |
理論分解電圧とは、アノードとカソードの平衡電位の差であって、槽電圧(浴電圧)をこれ以下に切り下げることはできません 。
11 )| プロセス | アルミニウム電解精錬 | 食塩電化イオン交換膜法 | 銅電解精製 | 亜鉛電解採取 |
|---|---|---|---|---|
| 理論電気量(kA・h/t) | 2980 | 670 | 844 | 820 |
| 理論分解電圧(V) | 1.17 | 2.2 | 0.1mV | 2.0 |
| 理論電解電力(kW・h/t) | 3490 | 1470 | 0.084 | 1640 |
| アノード電流密度(A/m(2) | 8000 | 3000 | 220 | 450 |
| 単槽電圧(V) | 4.0 | 3.15 | 0.31 | 3.3 |
| 電気量原単位(kA・h/t) | 3350 | 700 | 920 | 910 |
| 電解電力(kW・h/t) | 13400 | 2200 | 284 | 3000 |
| 電流効率(%) | 90 | 96 | 97 | 90 |
| 電圧効率(%) | 29 | 70 | 3.2×10-4 | 61 |
| エネルギー効率(%) | 26 | 67 | 3.2×10-4 | -55 |
| 物理量 | 単位 | 凡例 |
|---|---|---|
| 電極間距離 d | m | 電界の強さ=電圧÷電極間距離 |
| セル断面積 S | m² | 拡面倍率1で、平板モデルのとき電極面積≒セル断面積 |
| 電極面積 A | m² | 実験室でよく使う旗型電極の電極面積は 1cm²。 |
| セル定数a | 1/m |
セル定数a=電極間距離d÷セル断面積S コンダクタンス G = 導電率 σ ÷セル定数 電気抵抗 =抵抗率ρ×セル定数a |
| バルク電流密度j | A/m2 | バルク 電流密度 j = 電流I÷セル断面積 |
| 界面電流密度j | A/m2 | 界面 電流密度 j = 電流I÷電極面積 |
| 電界の強さe | V/m | 電界の強さe = 電圧V÷電極間距離 |
電流密度は、 工業電解やめっきの電解条件として設定され、 バトラー・ボルマーの式などで使います。
| 表面処理の種類 | 説明 | |
|---|---|---|
| 塗装 | 有機物を主体とする皮膜を形成 | トタン板(鉄|錫)、ブリキ板(鉄|亜鉛) |
| めっき | 金属の皮膜を形成 | |
| ほうろう | 素地金属に顔料を混入したガラス質の釉薬を焼きづける |
ある金属を別の金属薄膜で覆う技術をめっきといいます。 めっきはアノード酸化などとならぶ重要な表面技術です。 カソード の表面に金属を電解析出させるめっきを電解めっきと言います。 電気を使わず還元剤を使うめっきを無電解めっきと言います。 溶かした金属にどぶづけするめっきもあります。 すずをめっきして 腐食 しないようにした鉄板をブリキ板、 亜鉛をめっきして傷がついたとき亜鉛が犠牲になって鉄板を守るようにしたのをトタン板と言います。
| 表面処理法 | 目的 | 用途(具体例) |
|---|---|---|
| 電気めっき | (イ)装飾 (ロ)耐食 (ハ)耐摩耗 (二)機能 | |
| 無電解めっき | (イ)装飾 (二)機能 | |
| 気相めっき | (ロ)耐食 (ハ)耐摩耗 (ハ)機能 | |
| エッチング | (二)機能 | |
| アノード酸化 化成 | (イ)装飾 (ロ)耐食 (ハ)耐摩耗 (二)機能 | |
| 電解研磨 | (イ)装飾 (ロ) 耐食 (二)機能 | |
| 化学処理 | (イ)装飾 | (イ)装飾品(カラーステンレス) |
| 泳動電着 | (イ)装飾 (ロ) 耐食 (二)機能 | |
| 表面硬化
|
(ロ)耐食 (ハ)耐摩耗 | (ロ)+(ハ)耐食・耐摩耗品(工具) |
| 化学修飾 | (二)電極の機能化(電池用電極、センサー) | |
| 電鋳 | (イ)装飾 (二)機能 |
ハルセル試験では、 アノード に対して、 カソード を傾けることで、一回の電解実験で、さまざまな電流密度におけるめっき状態を確かめることができます。
銅めっき 米沢高等工業学校本館から 銀電量計を探してみよう。
アノードもカソードも銅だったら、理論分解電圧は何Vになるか?