 🏠
🏠
 🏠
🏠
| 分類 | 材料 | 特徴 |
|---|---|---|
| 電極材料 | 正極材料 (活物質) | 極性固体、 酸化物、 イオン結合、 絶縁体 |
| 負極材料 (活物質) | 極性固体(金属やグラファイト)/非極性固体(酸化物) | |
| 導電材 | 非極性固体 炭素材料 | |
| 分散剤 | 界面活性剤 | |
| ◇ バインダー | 界面活性剤 | |
| CMC・増粘剤 | 極性材料 | |
| 集電体 (金属) | 非極性固体 | |
| 電解質 | 電解液、添加剤* | |
| セパレータ | ||
| その他 | 外包材・リードタブ |
界面は、 極性どうし、あるいは非極性どうし、だとなじみがいい。 異なる界面では、なじみが悪いので、界面活性剤などを検討する。
96485.332 〔 C/mol 〕 は、アボガドロ数×電気素量で、それらはSIで定められた 定義定数 です。
工業的には、 26.801 〔 Ah/mol 〕をよく使います。
ファラデー定数は、 エネルギー密度や理論容量の計算にも使います。
正極活物質の反応は、 大きく均一固相反応と二相反応に分類されます。 MnO2やLCOは、均一固相反応と言えます。NiOOHやLFOは二相反応と言えます。 均一固相反応の放電曲線はS字型を描き、二相反応の放電曲線はL字型を描きます。 放電深さにおける起電力はネルンストの式で議論でいます。 バッテリーマネジメント の立場から言うと、S字型の放電曲線は、電圧だけで 残量管理ができるメリットがあります。 しかし負荷からすれば電池の電圧が変動してしまうデメリットもあります。
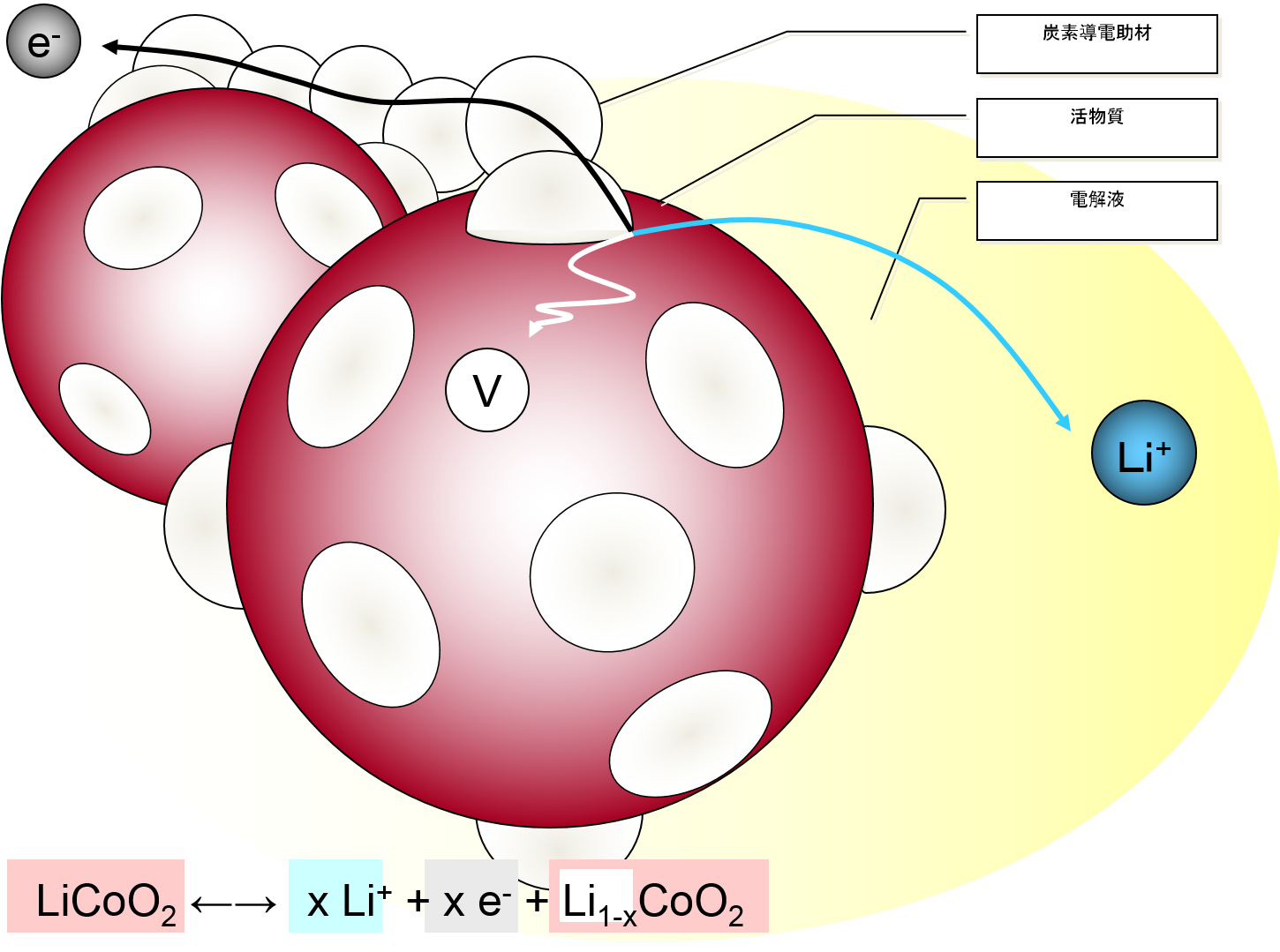
合材電極内部の活物質表面には、導電助剤、電解液、活物質の三相界面がある。 充電時には、電子が電子パスの導電助剤へ、リチウムイオンがイオンパスの電解液へ、そして空孔(ベーカンシー)が活物質バルクへと移動する。
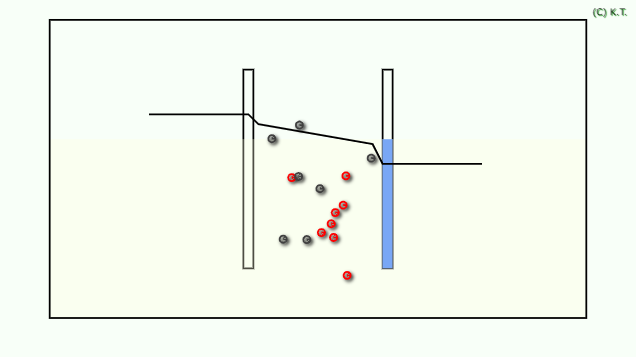
導電率は、 物性値です。 ベクトル量なので、導電異方性があれば、方向依存性があります。
導電率は、電流密度を電界の強さの比です。 電界の強さは電位勾配であり、電位勾配を見るには位置に対して電位を示した電位プロファイルが便利です。
| 材料 | 導電率 / S/m | 抵抗率 / Ω・m | |
|---|---|---|---|
| 1M KCl aq | 11.00 | 0.09 | |
| 0.1M NaOH aq 2 ) | 2.20 | 0.45 | |
| 1M LiPF6/PC+DME(1:1mol) 3 ) | 1.59 | 0.63 | |
| 35wt%食塩水( 🏞 海水) 4 ) | 4.00 | 0.25 | |
| 水道水 5 ) | 0.01 | 100.00 |
電解液( 電解質) はイオン電導です。自由電子による 金属の電子伝導に較べて導電率は8桁ほど小さくなります。 電池の内部抵抗を減らすには、 電極面積を増やし、電極間距離を縮め、導電率の高い電解液を使います。
導電率は 物性値なので、材料の形状によりません。 かたや形状のない材料などありません。
アセチレンブラックは、リチウムイオン電池の正極導電助剤としてよく使われます。粒径が小さく、充填効率が良いのでエネルギー密度の向上が期待されるからです。ABの導電機構は、基本的にはグラファイトと同じです。六角網面が球状に重なったオニオン構造をとり、それがクラスターを作り、ABの一次粒子となっています。
カーボン材料の表面はほとんど水素です。 官能基は、解放型とラクトン型に分類されます。 官能基の分析は、熱分析などによりますが、精度を上げることは困難です 7 ) 。
🏞アセチレンブラック抵抗率は、 物性値です。 金属は、電流を流す用途で使うので、電気抵抗から損失を計算しやすいように抵抗率で表現し、 半導体や電解液は、キャリア濃度との関係から 導電率で表現することが多いです。
| 金属 | 元素 | 導電率 /108S/m | 抵抗率 /10-8Ω・m | |
|---|---|---|---|---|
| ⚛ 🜛 銀 | Ag [5s1] | 0.63 | 1.59 | |
| ⚛ 🜠 銅 | Cu[4s1] | 0.60 | 1.68 | |
| ⚛ 🜚 金 | Au [6s1] | 0.41 | 2.44 | |
| ⚛ 🜀 アルミニウム | Al[3p1] | 0.38 | 2.65 | |
| ⚛ 亜鉛 | Zn [4s2] | 0.17 | 6.02 | |
| 真鍮 (黄銅) | Cu,Zn | 0.14 | 7.00 |
電線ばかりでなく、 電池の集電体にも使われます。 リチウムイオン電池の 集電体には、銅とアルミニウムが使われます。
https://www.hata-cu.com/blog/post-309/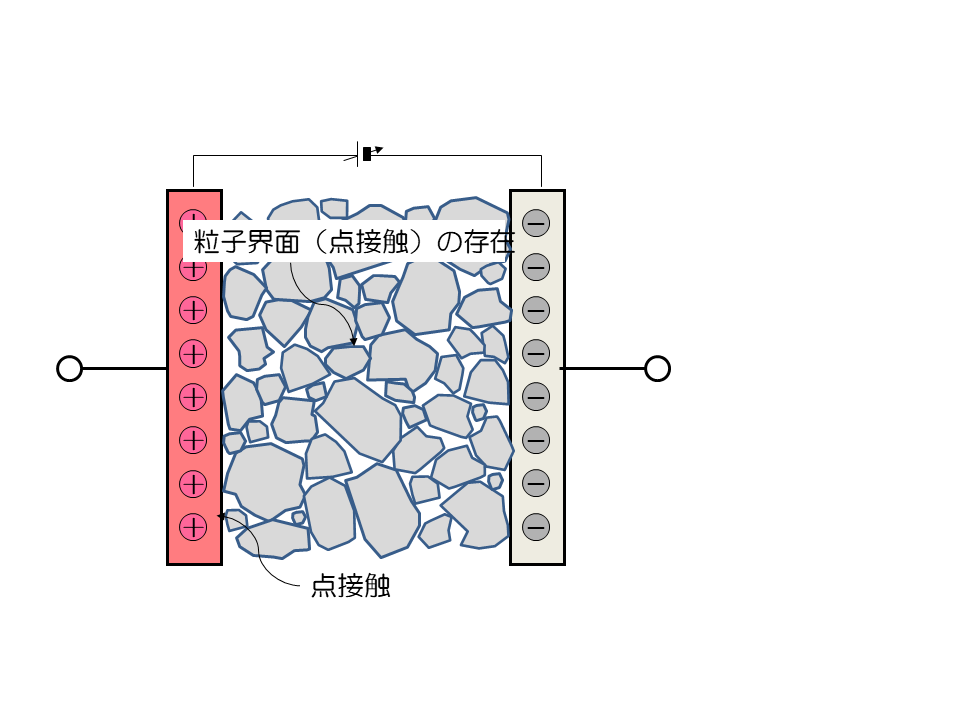
固体粒子の接触は、点接触です。面積を見積もるのがとても大変です。界面の電流密度がわかりません。 接触抵抗は電流集中( 集中抵抗)を伴うので、圧縮などの影響を受けやすいのです。活物質や炭素材料、固体電解質などの取り扱いが難しいのはそのためです。