 🏠
🏠
 🏠
🏠
電池の起電力と分解電圧は電気化学や学生実験でも触れたけど、もういちど理解を深めてみよう

てのひらに、10円と1円をのせれば、 電気化学の三要素 がそろって、電池になります。 デジタル式回路計で、 電圧を測定すると、0ではありません。 これが 電池の起電力です。 電流が流れていないにもかかわらず電圧があるのです。 電池では、電流と電圧が、そのまま比例しません。 電池は単なる電気抵抗ではないのです。 化学反応が電気を起こしているのです。 11円電池は、 ガルバニ電池と言っていいでしょう。
酸化体が多いほど、酸化力(電位)が上がります。 電位は、ネルンストの式で説明されます。
電気量が物質量に対応するとしたら、電位は物質の酸化力に対応します。厳密には酸化力は物質と物質の相対的な関係で決まるので、平衡反応に対応することになります。 とは言え Fe3+ と Fe2+ が混ざっていたら、 Fe3+ が多い方が電位が高くなります。 このことを定量的に示したのがネルンストの式です 2 ) 3 ) 。

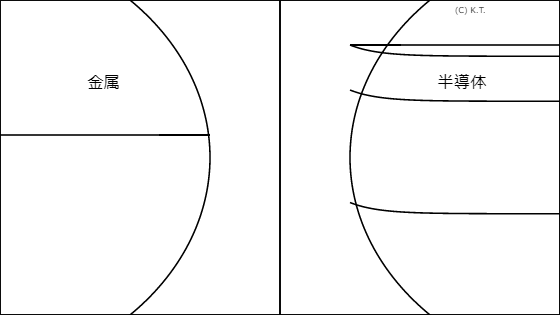
LUMOは、最低空分子オービタル。 HOMOは、最高被占分子オービタル。 基本的にHOMOが高いほど酸化されやすく(酸化還元電位が低い)、LUMOが低いほど還元されやすい(酸化還元電位が高い)。
LUMOのエネルギー準位と HOMOのエネルギー準位とのあいだに フェルミ準位があると思っていい。
Fe3+/Fe2+の半反応式は次式で表されている.この半反応式の 酸化還元電位は標準水素電極(NHE)に対し +0.771 Vである.
分解電圧を調べるときは、電圧を掃引して、電流を測定します。 これを LSV (リニアスイープボルタンメトリー)ということもあります。 電流電圧曲線から、溶液抵抗の傾きを外挿して、分解電圧を求めます。 理論分解電圧から分解電圧を引いて、 過電圧を求めます。 過電圧を電流密度の対数の関係をターフェルプロットと言います。
電池では、電流を掃引して、電圧を測定します。 求めた電流電圧曲線は、電池の放電の 内部抵抗 を求めるのに使われます。
| 固体 | 液体 | 気体(真空) | |
|---|---|---|---|
| 固体 |
面接触(例:
pn接合) 線接触(三相界面)(例:正極合材、 局部電池) 点接触(三相界面 ショットキー接触 )(例:固体電解質、 炭素導電助剤粒子 ) |
固液界面 (例:サスペンジョン) | 表面 |
| 液体 | 固液界面 (例:電極と電解液) | 液液界面 (例:エマルション) | 気液界面 ( 表面 ) |
| 気体(真空) | 表面 | 気液界面 ( 表面 ) | (混合) |
物質は、 様々な状態をとります。 界面や表面 は、ある材料の相と異なる材料の相が接するところです。
電池の内部抵抗は、バルクと界面との両方から生じます。

空間電荷層を含みます。
| 例 | 備考 | |
|---|---|---|
| 銀|塩化銀電極 | AgCl + e- ↔ Ag + Cl- Eº = 0.2223V* | 温度、 Cl-濃度に依存 |
| 水銀|塩化水銀電極 | Hg2Cl2 + 2e- ↔ 2Hg(l) + 2Cl- Eº = 0.26816V * | 温度、Cl-濃度に依存 |
| 水銀|酸化水銀電極 | HgO + H2O + 2e- ↔ Hg(l) + 2OH- Eº = 0.0977V * | アルカリ用(アルカリ電池の研究、粘土分散液の研究)、温度、OH-濃度に依存 |
| 水銀|硫酸水銀電極 | Hg2SO4 + 2e- ↔ 2Hg(l) + SO42- Eº = 0.613V * | 酸性用(鉛電池の研究、二酸化マンガンの電解合成の研究)、温度、SO42-濃度に依存 |
「椅子を高く持ち上げたときに消費するエネルギーは、椅子の位置エネルギーに時間をかけて求めることができる」はほんとうか?? 問
銅の電解精錬に使う電力は何のためか?それを節電するにはどうしたらいいか?注意すべき点は何か?? 問
