3ボルトが生み出す塩と水素―電気化学工業―. 山形大学, 無機工業化学 講義ノート, 2016. https://edu.yz.yamagata-u.ac.jp/developer/Asp/Youzan/@Lecture.asp?nLectureID=4484 , (参照 ).
 🏠
🏠
 🏠
🏠
3ボルトが生み出す塩と水素―電気化学工業―. 山形大学, 無機工業化学 講義ノート, 2016. https://edu.yz.yamagata-u.ac.jp/developer/Asp/Youzan/@Lecture.asp?nLectureID=4484 , (参照 ).
新型コロナウイルス感染症(COVID-19)感染拡大防止のため、抗ウイルスを謳った商品が巷にあふれている。抗ウイルス材料には、有機物、無機物、それぞれにさまざまなものがある。ネットで検索すると、効能書きがあるものの、その根拠となるデータに乏しいものも少なくない。またその作用機序について系統的に発信している情報も見当たらない。 たとえば消毒に次亜塩素酸水が使われている。塩化ナトリウム水溶液を電気分解した「電気分解方式」や次亜塩素酸ナトリウムと塩酸などを混ぜ、酸性したものは、安定性に乏しく、長期保存できない。それに対して二酸化炭素を混ぜ、重炭酸イオンで緩衝作用を持たせたものは、安定である。しかし、その安定化機構や作用機序については十分に解明されているとは言えない。
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/syoudoku_00001.html次亜塩素酸水は、 次亜塩素酸の混合物です。
【参考情報2 「次亜塩素酸ナトリウム」と「次亜塩素酸水」について】 「次亜塩素酸ナトリウム」と「次亜塩素酸水」は、名前が似ていますが、異なる物質ですので、混同しないようにしてください。 「次亜塩素酸ナトリウム」は、アルカリ性で、酸化作用を持ちつつ、原液で長期保存ができるようになっています。ハイターなどの塩素系漂白剤が代表例です。 「次亜塩素酸水」は、酸性で、「次亜塩素酸ナトリウム」と比べて不安定であり、短時間で酸化させる効果がある反面、保存状態次第では時間と共に急速に効果が無くなります。 「次亜塩素酸水」にはいくつかの製法がありますが、このうち、食塩水や塩酸を電気分解して生成した「次亜塩素酸水」には、食品添加物(殺菌料)に指定され、規格が定められたものもあり、食品加工工場における野菜の洗浄などに使われます。 また、次亜塩素酸ナトリウムを原料に、酸を加えたり、イオン交換等をすることで酸性に調整したものも「次亜塩素酸水」として販売されています。これには規格や基準が無く、成分がはっきりしないものもあります。また、「pHを調整した次亜塩素酸ナトリウム」と称して販売する例があり、アルカリ性の「次亜塩素酸ナトリウム」と酸性の「次亜塩素酸水」の混同の一因になっています。
次亜塩素酸 次亜塩素酸の酸化力 プロジェクト
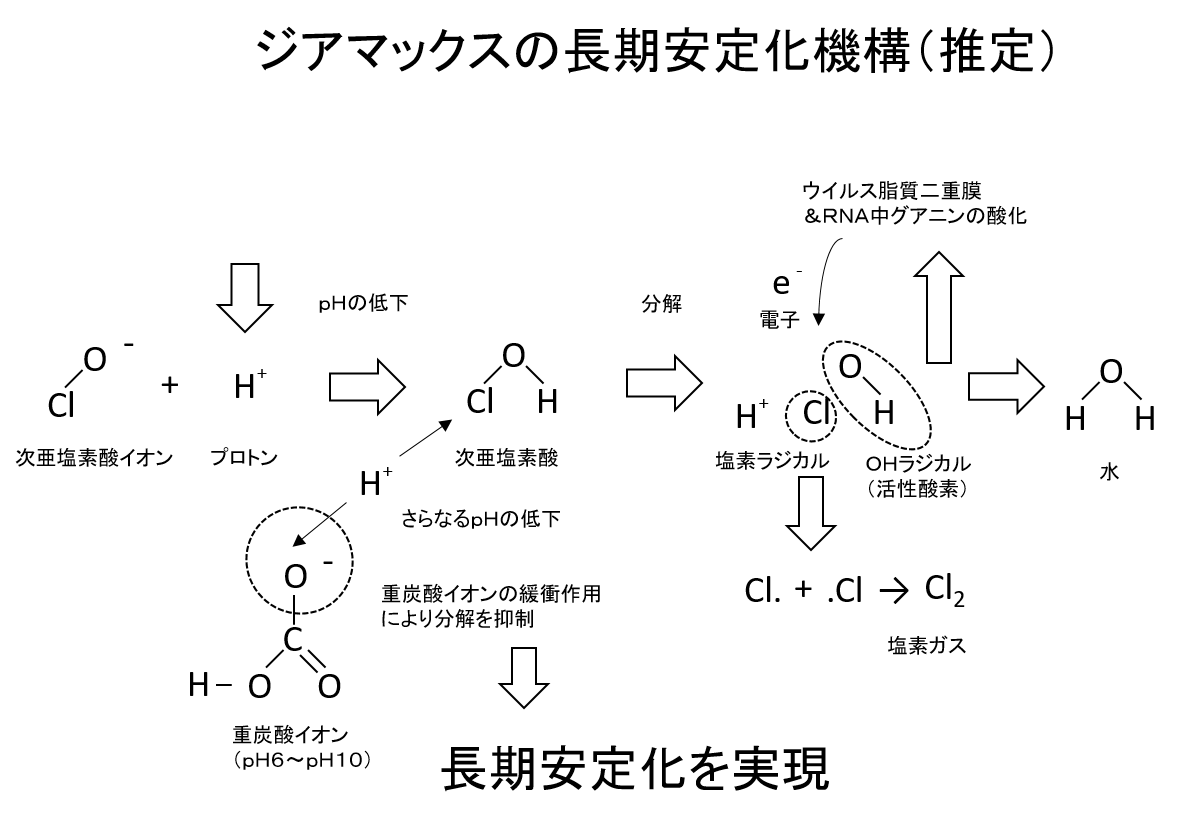
図1に示すように次亜塩素酸では、塩素原子は一価のプラスの原子価を持ち、水分子における水素原子のひとつを塩素原子で置き換えたような分子である。アルカリ性の水溶液中では、次亜塩素酸は、次亜塩素酸イオンとプロトンとに乖離する。この平衡はpHが大きいほど促進される。

OH・の酸化還元電位?直接的に見たわけではないので,あくまで,推定になります. 水に電位をかけると書いてあるのですが,起きる反応としては,下記が推定されます. 推察でしかありませがん,TiO2のメカニズムからしても,水に電子を与えて,OHラジカルを 生成する電位が+2.58Vとい意味かと捉えています.
H3O+ + e(-) <-> H2 + OH・
鉄と過酸化水素の反応系では,フェントン反応が有名で, 連鎖的に反応し,最終的に過酸化水素が生成されたような気がします.
Fe(II)1) + H2O22) → HO・3) + HO-4) + Fe(III)5)6)
Fe(II) + HO・ → Fe(III) + HO- 7)
H2O2 + HO・ → HOO. + H2O
DMPO8) + HO. → DMPO-OH.9)10)
【化学種ヒドロキシルラジカル】 https://a.yamagata-u.ac.jp/amenity/electrochem/species/SpeciesWeb.aspx?nSpeciesID=1619 【フェントン反応】 https://a.yamagata-u.ac.jp/amenity/Keyword/KeywordWeb.aspx?nKeywordID=5232 【スーパーオキシドアニオンラジカル】 https://a.yamagata-u.ac.jp/amenity/electrochem/species/SpeciesWeb.aspx?nSpeciesID=282 3時まで時間がないので,取り急ぎ,ご返事まで. 2020年5月15日(金) 10:42