2018/07/02 輪講
メディエイターを用いた酵素の電極反応
どんな分子でもメディエイター分子になれるわけではない。各々の酵素にはそれぞれに適したメディエイター分子がある。
GODと同じフラビン部位を活性中心とするフラビン蛋白質でもアミノ酸であるサルコシンの酸化酵素や乳酸の酸化酵素は、
それぞれGODに有効なメディエイターよりもむしろモリブデンやタングステンのシアノ錯体が有効なメディエイターとなる
ことが知られている(図1)。適切なメディエイターを捜すことは必ずしも容易ではないが、メディエイター分子の酸化還元
電位、分子の形、親水性、疎水性、電化状態などが重要で、おそらく酵素の活性中心に接近でき、電子授受を行うのに適し
た条件が要求されるのであろう。酵素は適切なメディエイターがあれば、電気化学的に酸化(あるいは還元)できるので(
この場合酸素がなくても働く)これを利用したセンサや酵素反応を利用した合成反応電極をつくることができる。また、電
気化学の手法を利用して酵素反応の過程を解析し、酵素反応を特徴付けるミカエリス定数や反応速度を求めることもできる。
すなわち、一般にメディエイターを用いた溶液内での酵素反応速度(v)は、
v=k[E]/(1+KS/[S]n+KM/[M]n) (1)
ここでkは速度定数(s-1)でvmax=k[E]、KS
およびKMはそれぞれ基質及びメディエイターに対する酵素反応のミカエリス定数(酵素と基質の複合体の
解離定数=[E]・[S]/[ES]に相当し、酵素反応の最大速度vmaxの1/2の速度の時の基質濃度)、[E]、[S]、
[M]は酵素、基質、メディエイターの濃度を表す。nは通常1(または2)である。図1(c)の場合の電流がどれだけ大きく
なるかを種々の条件下で測定することによって上記のパラメーターが評価できる。このようにメディエイターを用いることで、
酵素反応を外から電気化学的に制御することができるようになる。
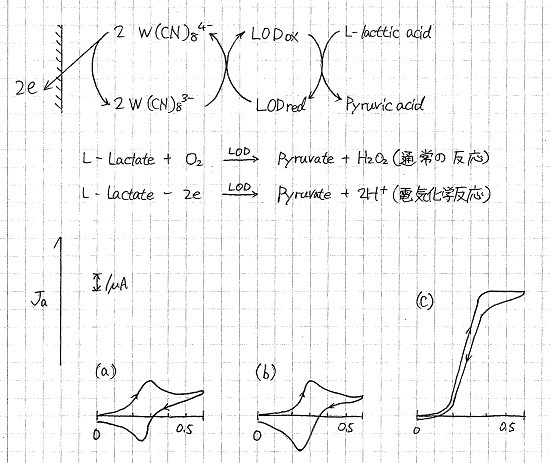 図1 乳酸酸化酵素-(LOD)-メディエイター系のボルタモグラム
図1 乳酸酸化酵素-(LOD)-メディエイター系のボルタモグラム
(a) 0.5mM K4[W(CN)8];
(b) a)+1.7μM LOD;
(c) b)+30mM L-乳酸(メディエイターの酸化電流の増加がみられる触媒電流)
溶液は、0.1M KClを含むリン酸緩衝液(pH7). 25℃. N2下。電位掃引速度 1mV/s
I. Tanigucti, et al., J. Electroanal. Chem., 240, 333 (1988)
参考文献
山下正通ら. 現代の電気化学. 初版, 新星社, 1990, 329p.
戻る

