電池の評価法~交流インピーダンス法. 山形大学, 電気化学特論 講義ノート, 2012. https://edu.yz.yamagata-u.ac.jp/developer/Asp/Youzan/@Lecture.asp?nLectureID=4046 , (参照 ).
 🏠
🏠
 🏠
🏠
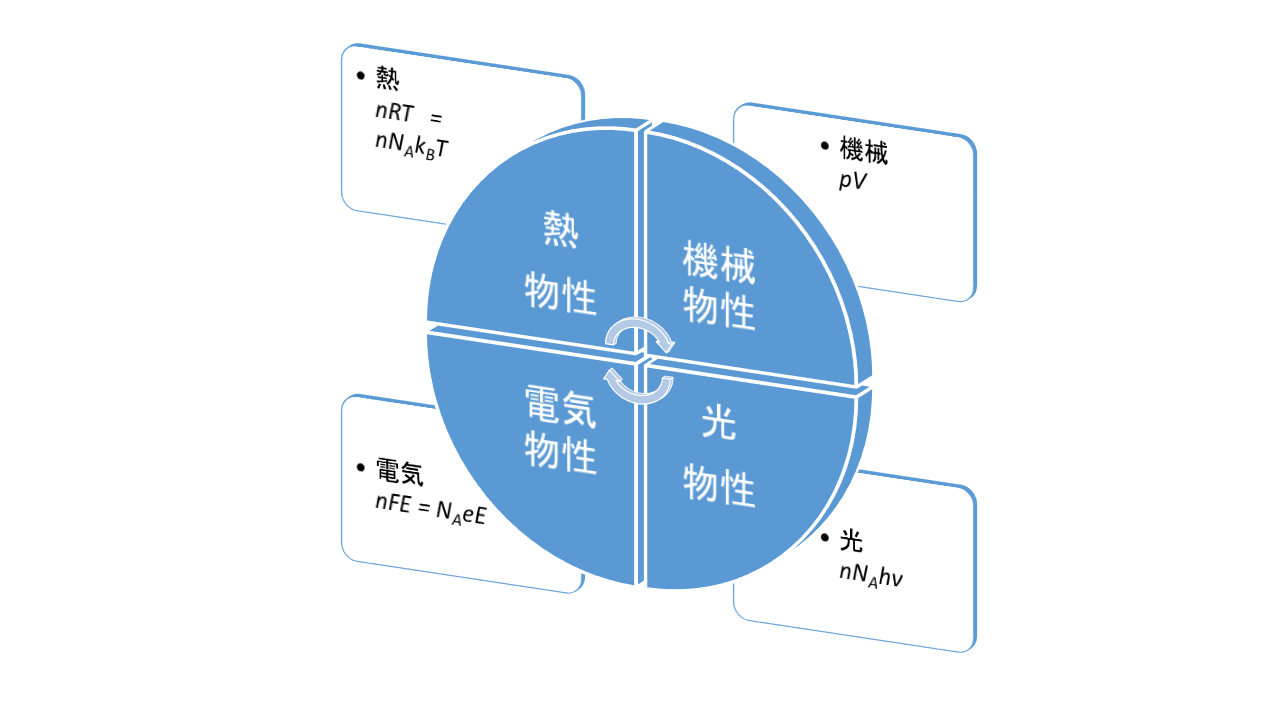
物性には、 熱物性、 機械物性、 電気物性、 光物性がある。 それぞれ、熱エネルギーに対して物質が
スペクトルでは、波長の短い青の方がエネルギーが大きく、波長の長い赤の方がエネルギーが小さいです。ストーブをがんがん燃やしても、日焼けせず、ちょっと日を浴びるとすぐ日焼けするのはそのためです。
| 物質 | |||
|---|---|---|---|
| 電解製造 | 電解採取 | 水溶液 : 🏞 🧪 ⚛ 塩素 、 🏞 苛性ソーダ、 (食塩電解) 🏞水素 、 ⚛ 亜鉛 | |
| 溶融塩 : 🏞 ⚛ アルミニウム | |||
| 電解合成 | 水溶液 :二酸化マンガン | ||
| 有機物 :アジポニトル | |||
| 電解精製 | 銅 | ||
| 電気透析 | 🏞 食塩 |
洗剤や漂白剤は液体の化学薬品がそのまま身近な生活に使われます。 温度と圧力で作ることができる液体や気体は灰汁やアンモニアです。 今やぼくらは電気の力を化学に使うことができる。 それが電解です。 加熱や加圧の 単位操作だけでは作れなかった化学薬品を手に入れましょう。
1 ) 2 )| kWh、 J | 関係式 | 示強性変数 | 示量性変数 | 物質量あたり マクロ |
粒子あたり ミクロ |
|---|---|---|---|---|---|
| 🧪 化学エネルギーG | ⊿G=⊿H-T⊿S | 化学ポテンシャル | 物質量〔mol〕 | アボガドロ数
NA |
|
| 🔥 熱エネルギー |
🖱
Q=
TS
RT
|
温度 T 〔K〕 | エントロピー S 〔J/K〕 | 気体定数 R 〔J/K・mol〕 | ボルツマン定数 kB 〔J/K |
| 💪 力学的エネルギー E | 🖱 W=pV | 圧力 p 〔Pa〕 | 体積 V 〔m3〕 | 理想気体のモル体積 x 〔L/mol〕 | |
| ⚡ 電気エネルギー E |
🖱
E=VQ
E=nFE
|
電圧 V 〔V〕 | 電気量 Q 〔C〕 | ファラデー定数 F 〔C/mol〕 | 電気素量 e 〔C〕 |
| 🌟 光エネルギー E | E=hν | 振動数 ν 〔Hz〕 | プランク定数 h 〔J・s〕 |
エネルギーは、相互に エネルギー変換できます。 エネルギーは保存則でなくなりませんが、有効な仕事として利用できるエネルギー(エクセルギー)の割合は減っていき、廃熱(アネルギー)の割合が増えていきます。 その意味で、熱エネルギーはエネルギーの廃棄物と言えます。
状態量物質は、 温度や圧力 によって、様々な状態をとります。 物質が固体、液体、気体、 超臨界流体のいずれの 状態を示した図を 状態図と言います。 分子結晶は、昇華しやすく、 イオン結晶は、融点や沸点が高いです。
| 金属材料 | 非金属材料 | 複合材料 | ||
|---|---|---|---|---|
| 鉄鋼材料 | 非鉄金属材料 |
セラミックス ガラス |
高分子 ゴム |
|
|
炭素鋼
合金鋼
鋳鉄
鋳鋼
|
金・銀
・
銅
アルミニウム
マグネシウム
ニッケル
チタン
亜鉛
|
🏞
石材
|
繊維強化プラスチック
繊維強化金属
鉄筋コンクリート
金属強化セラミックス
|
|
材料は、その材質の違いにより金属材料と非金属材料に分類されます 3 ) 。
狭い意味で、材料といったとき、常温常圧で固体の 状態の 物質を指すことがあります。
純物質としての 金属は、柔らかすぎるので、混合物の合金が使われます。広い意味での混合物の固体材料を複合材料と呼ぶことがあります。
水は、10-7程度は、H+とOH-に乖離している。これをオートプロトリシスと言う。 水の中の酸素原子と水素原子の結合は、共有結合だろうか?イオン結合だろうか?
ケイ酸塩は、ケイ素原子を酸素原子を取り囲んだ構造になっている。 ケイ酸塩とはいうものの、ケイ酸イオンの状態はほとんど存在しないと言っていい。 ケイ酸塩中の、ケイ素原子を酸素原子の結合は、共有結合だろうか?イオン結合だろうか?
| 結合の種類 | 結晶 | 性質や特色 | 物質の例 |
|---|---|---|---|
| イオン結合 | イオン結晶 | 固体 は 導電率が小さい(絶縁体)。水溶液や溶融塩は 導電率が大きい。 (キャリア:イオン)。 | 塩化ナトリウム、塩化銀、水酸化ナトリウム |
| 共有結合 | 分子結晶 | 分子式 で表す。融点や沸点は低い。 | 酸素、アンモニア、水※1、ドライアイス |
| 共有結合の結晶 | 黒鉛や導電性高分子は、例外的に電気を通す。 | ダイヤモンド、 黒鉛、 ケイ素、 水晶 、石英※2 | |
| 金属結合 | 金属の結晶 | 導電率 が大きい(キャリア:自由電子)。 | 銅、亜鉛、 🜀 アルミニウム リチウム |
※1.水分子は共有結合に分類されるが、液体の水はわずかに電離して電気を流す。 このイオン結合的な性質を、極性分子と表現する。
※2.ケイ酸塩のケイ酸はイオン結合に分類されるが、共有結合としての性質が強く、焼成などで成型することができる。
電気を流すのは金属だけと思ってよい。それ以外に電気を流すのは特例である。
https://www.hakko.co.jp/qa/qakit/html/h01100.htm導体としては金属や合金が一般的であり、CuやAlなどの金属は送電用ケーブルに使用される。
最新工業化学―持続的社会に向けて―より引用
現在の山形大学の使用電力は下記の図に示したとおりです。
純粋な水は、ほとんど電気を流さない。 でも、高電圧をかければ純水でも電気分解ができるのだろうか?
電気が流れるのは電気を運ぶ何かが移動するからである。この電気を運ぶ何かをキャリア(担体)と言う。 キャリアには電子とイオンがある。金属は電子伝導、電解液はイオン伝導である。 欠陥がキャリアになることもある。電子の欠陥はホール(正孔)であり、イオンの抜け穴はベーカンシー(空孔)と呼ばれる。

| 形態 | 説明 | 流動 | |
|---|---|---|---|
| 対流 | 重力・動力(撹拌) | ||
| 🖱 泳動 | 電位勾配/ クーロン力/導電率 | 位置エネルギーを最小に | 慣性支配 |
| 🖱 拡散 | 濃度勾配/拡散係数 | エントロピーを最大に 拡散方程式 拡散過電圧 | 粘性支配 |
拡散と対流は、イオン移動だけでなく物質移動でも起こります。拡散はイオン移動だけでなく 熱移動でも起こります。
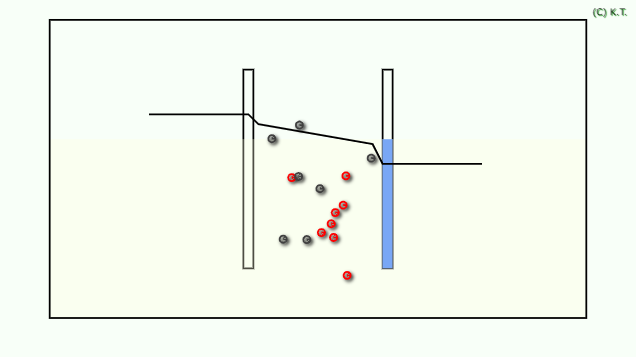
導電率は、 物性値です。 ベクトル量なので、導電異方性があれば、方向依存性があります。
導電率は、電流密度を電界の強さの比です。 電界の強さは電位勾配であり、電位勾配を見るには位置に対して電位を示した電位プロファイルが便利です。
書きかけです
書きかけです

空気は電気を流しません。流そうとすると1センチあたり3万ボルトの電圧が必要です。
真空は電気を流します。
| 分類 | 状態 | 性質や特色 | 物質の例 |
|---|---|---|---|
| 気体 | プラズマ | 電離したイオンと電子が動く | 雷 |
| 液体 | 電解質溶液 | イオン結晶が、溶媒中で、電離し、 溶媒中を溶媒和したイオンが 泳動 | 食塩水, KOH aq, LiPF6/EC+DEC |
| 溶融塩、イオン液体 | イオンが泳動 | LiCO3+KCO3 | |
| 固体 | ゲル電解質 | 溶媒で膨潤したマトリクス中をイオンが 泳動 | PVdF? |
| 固体電解質 | 固定された格子中をカチオンが半融状態で 泳動 | AgI LiF(SEI) ポリマー電解質 |
電気分解は、電解質(電子絶縁体)の絶縁破壊です。
| 材料 | 導電率 / S/m | 抵抗率 / Ω・m | |
|---|---|---|---|
| 1M KCl aq | 11.00 | 0.09 | |
| 0.1M NaOH aq 4 ) | 2.20 | 0.45 | |
| 1M LiPF6/PC+DME(1:1mol) 5 ) | 1.59 | 0.63 | |
| 35wt%食塩水( 🏞 海水) 6 ) | 4.00 | 0.25 | |
| 水道水 7 ) | 0.01 | 100.00 |
電解液( 電解質) はイオン電導です。自由電子による 金属の電子伝導に較べて導電率は8桁ほど小さくなります。 電池の内部抵抗を減らすには、電極面積を増やし、電極間距離を縮め、導電率の高い電解液を使います。
導電率は物性値なので、材料の形状によりません。 かたや形状のない材料などありません。
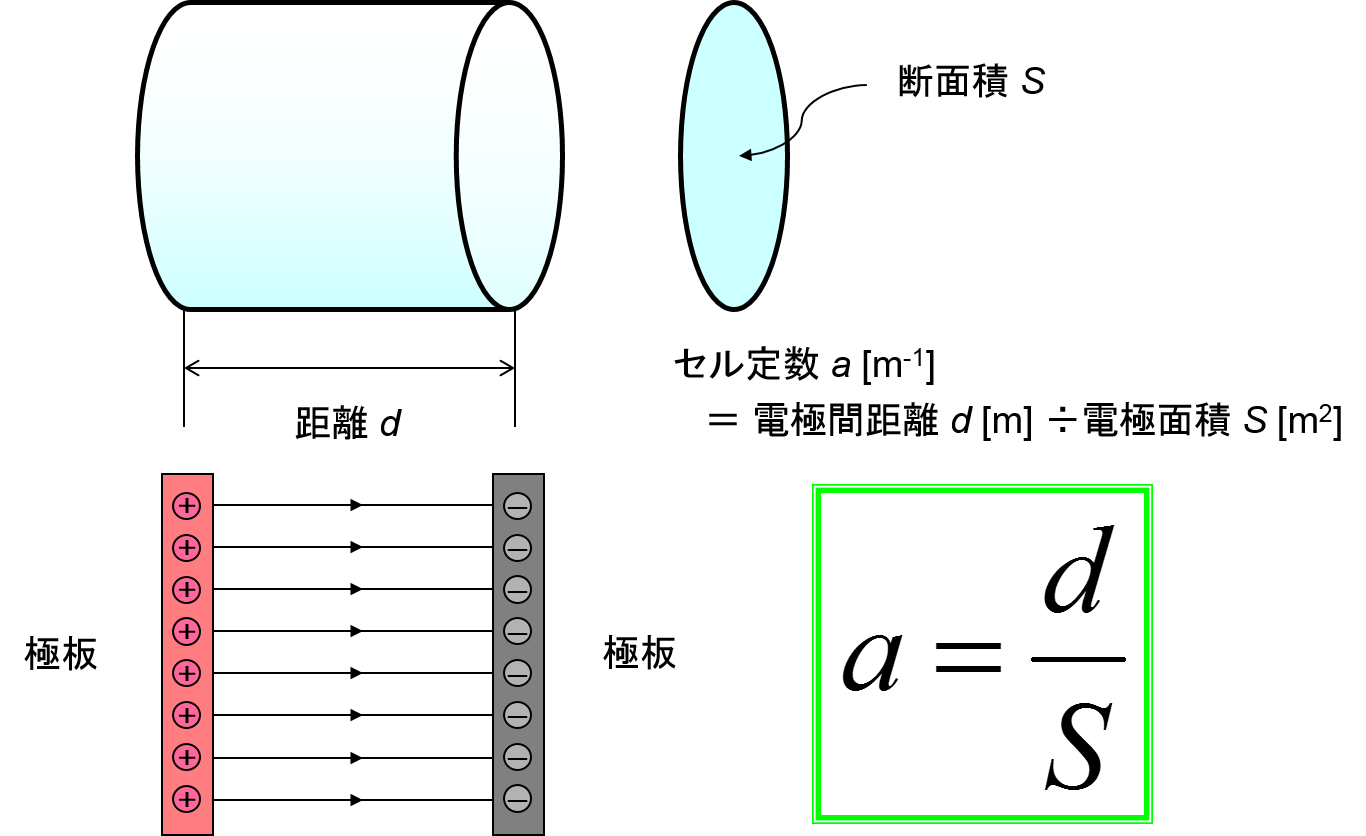

平行平板電極であれば、
セル定数a=電極間距離d÷セル断面積S
です。
一般的には、導電率既知のKCl溶液などを使って、セル定数を較正します。
コンダクタンス=導電率
電気抵抗=抵抗率×長さ÷電極面積
電池の評価法~交流インピーダンス法. 山形大学, 電気化学特論 講義ノート, 2012. https://edu.yz.yamagata-u.ac.jp/developer/Asp/Youzan/@Lecture.asp?nLectureID=4046 , (参照 ).
このマークは本説明資料に掲載している引用箇所以外の著作物について付けられたものです。
銅めっき 米沢高等工業学校本館から 銀電量計を探してみよう。
アノードもカソードも銅だったら、理論分解電圧は何Vになるか?
2024年1月21日 松木健三名誉教授がご逝去されました。