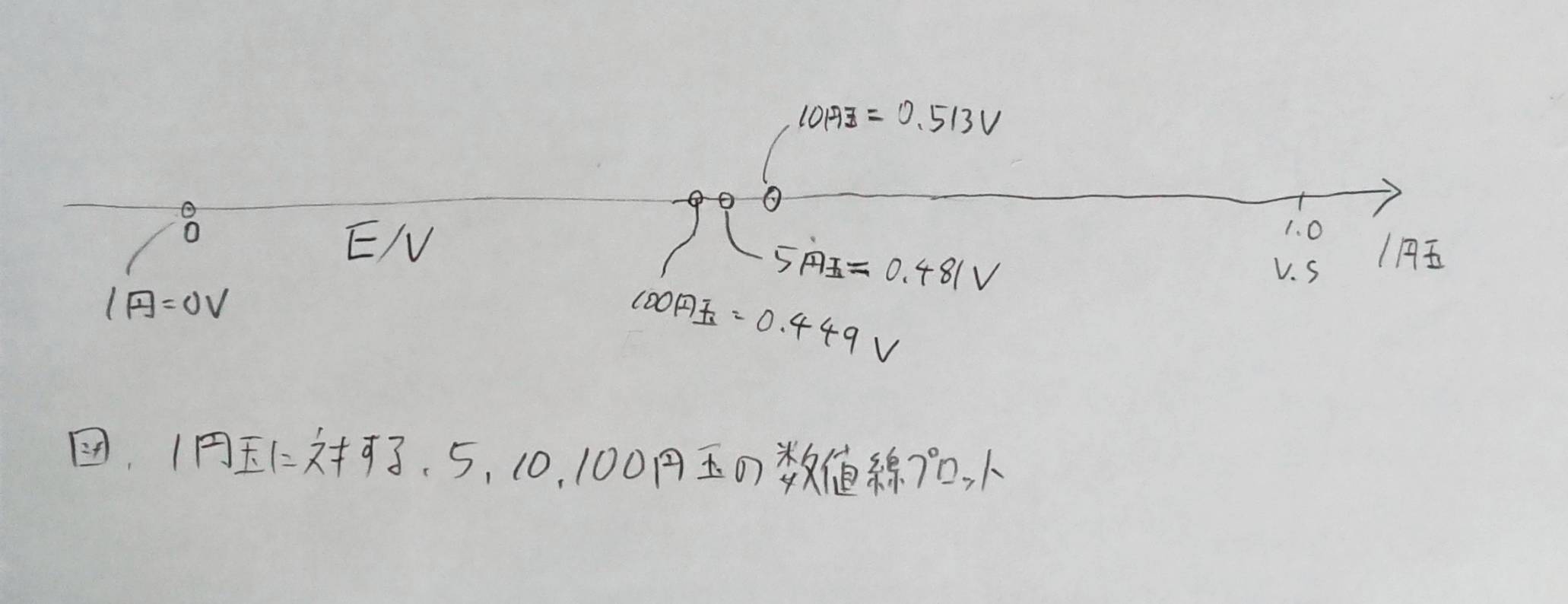
1円に対する各硬貨で作成した電池の電圧
100円 0.449V
10円 0.513V
5円 0.481V
コイン電離の電位プロット
自作したコイン電池

自作したコイン電池の測定

室温

室温は20.3℃であった。
ビーカー(電解セル) 2、セロハンチューブ、セロハンテープ、
硫酸銅、亜鉛線 1、銅線 1、クリップ、導線、電流計 1、電位差計、電圧計 1、
スイッチ、 銀線、3M HNO3 、0.1M HCl、白金、KCl、AgCl
1.ダニエル電池を組み立てと塩橋の作成
1.セロハンチューブとセロハンテープによる塩橋の作成
・セロハンチューブを片方のみが開くように、下部をセロハンテープで固定する。
・セロハンチューブの方側面を垂直方向に全体を少し折り、セロハンテープで固定する。
・銀線を紙やすりで削り、清浄な金属表面を露出させ、その金属表面を3M HNO3 で処理し、水洗いする。
電池式
(-)Zn|ZnSO4aq||CuSO4aq|Cu(+)
起電力 1.0964 V
Cu +0.337 V
Zn -0.7672 V
測定方法
・テスターなどの測定器の動作を確認する。電流計 1、電圧計 1、電解セル(ビーカー)、白金線 2、充電池 1、 抵抗尺 1、スイッチ 1、硫酸、水酸化ナトリウム、塩酸、銅線、亜鉛線、黒鉛棒、鉄線
セルを以下の式のように組み立てる。電解セルには10mLビーカーを用い、転倒防止のため両面テープで固定する。
Pt | H2SO4 | Pt
実験開始前にコイン電池に使用する効果が3種類しか無かったため、
はじめは、かなり焦ったが、なんとか用意することができたので、
結果的に冷静な行動をすることができた。